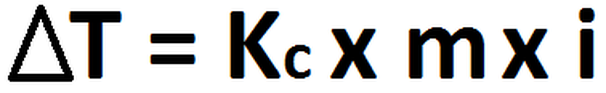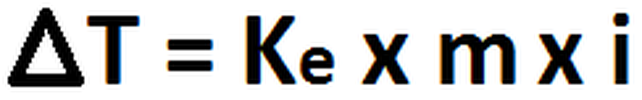Resultados
7.
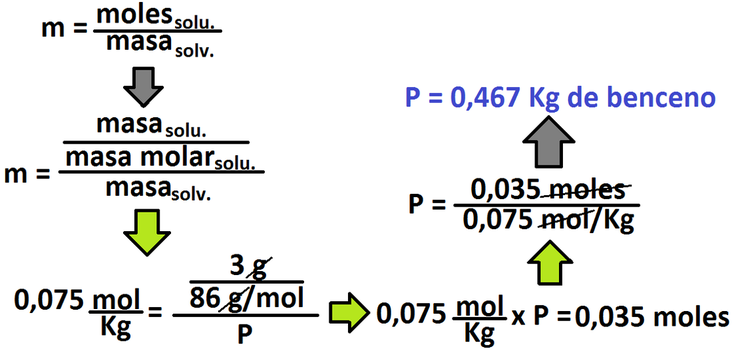
Para responder este tipo de problemas, se necesita saber la molalidad y la constante (sea ebulloscópica como crioscópica, siendo esta pultima la requerida ahora). El valor de la constante está dado, por lo que debemos averigual la molalidad de la disolución:
Para responder este tipo de problemas, se necesita saber la molalidad y la constante (sea ebulloscópica como crioscópica, siendo esta pultima la requerida ahora). El valor de la constante está dado, por lo que debemos averigual la molalidad de la disolución:
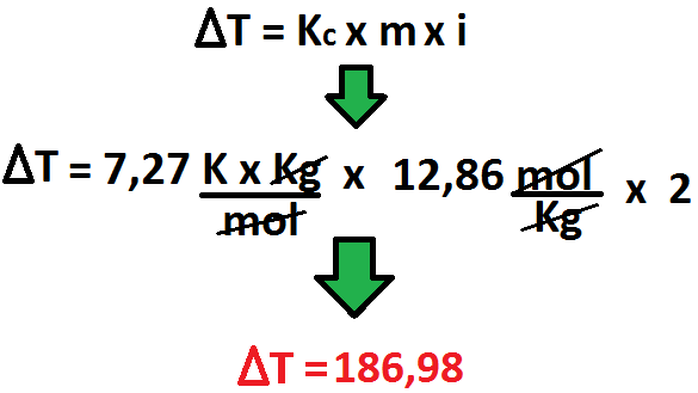
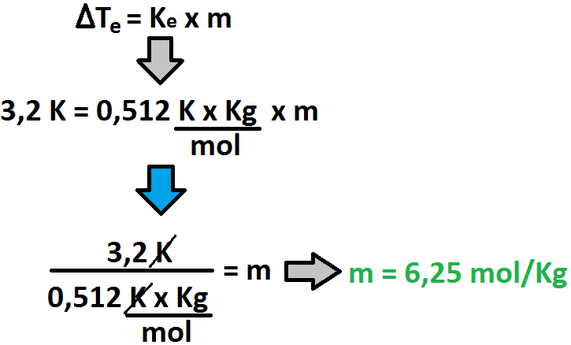
Ahora, calculemos la molalidad:
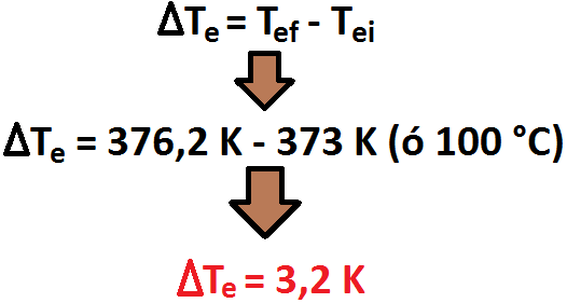
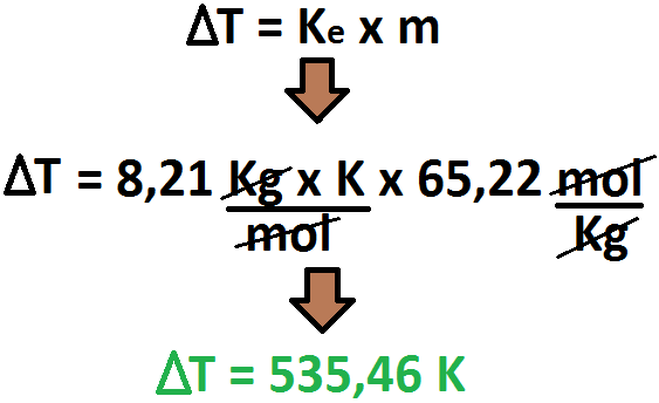
Por ende, el valor del cambio de temperatura de fusión sufrido por la disolución es de:
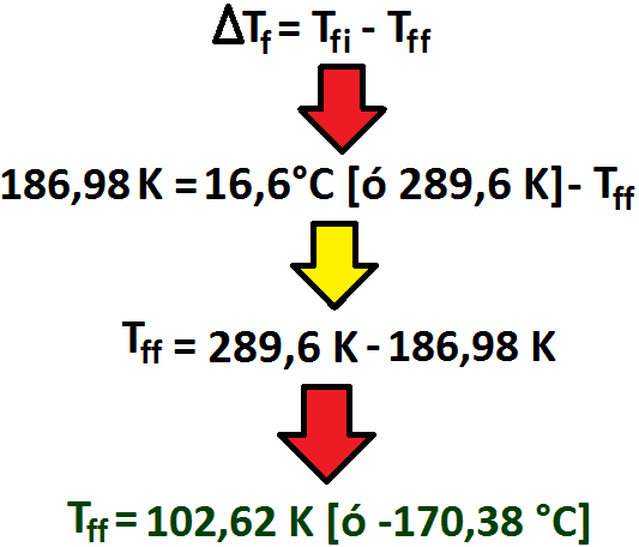
Como todos saben, el símbolo delta mayúscula (se representa por un triángulo) indica diferencia, es decir, se resta lo menor a lo
mayor, por ende, la respuesta final será:
A nosotros se nos pide calcular la cantidad de moles de soluto, para lo cual debemos calcular la molalidad primero. Para esto,
debiésemos tener la diferencia en la temperatura de ebullición y la Ke (ambos datos otorgados en el enunciado), por lo cual
quedaría:
Como i = 1, podríamos expresar la fómula necesaria para calcular el aumento ebulloscópico de la siguiente manera:
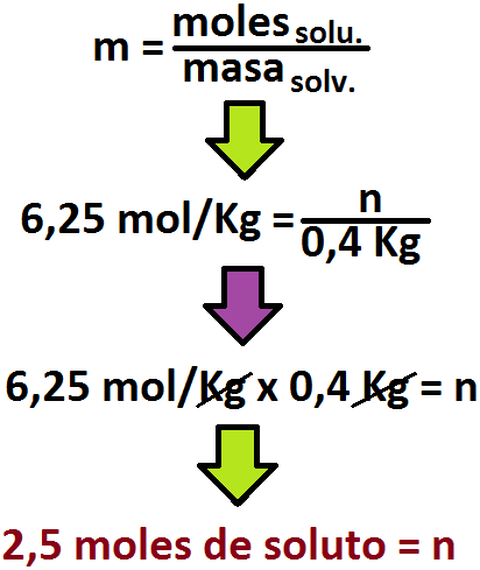
Como se tiene en el enunciado que la densidad del agua es de 1 g/mL, entonces podríamos decir que 400 mL = 400 g = 0,4 Kg de
agua, por ende se tendrá que la cantidad de moles de soluto será igual a:
9.
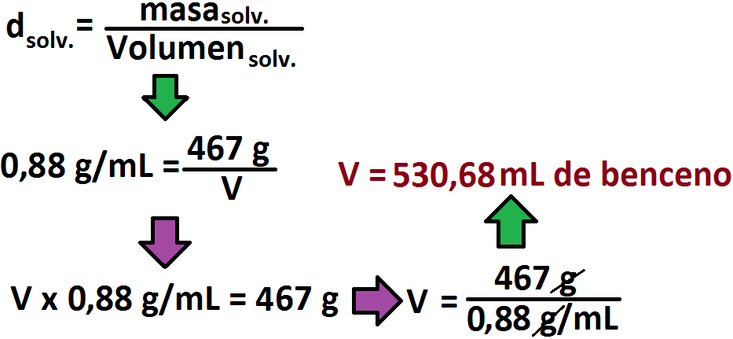
En esta pregunta se nos pregunta el volumen de benceno, el cuál corresponde al solvente. Para eso nos sería útil calcular el peso del solvente, ya que, como poseemos su densidad, el peso lo podremos convertir a volumen y así contestaremos la pregunta que se nos planteó. Como en ejercicios anteriores, omitiremos i en la fórmula ya que según el enunciado i = 1.
Como sabemos que 0,467 Kg = 467 g de solvente, podemos pasar esta masa a volumen mediante la densidad y responderemos de
esta manera el problema planteado:
10.
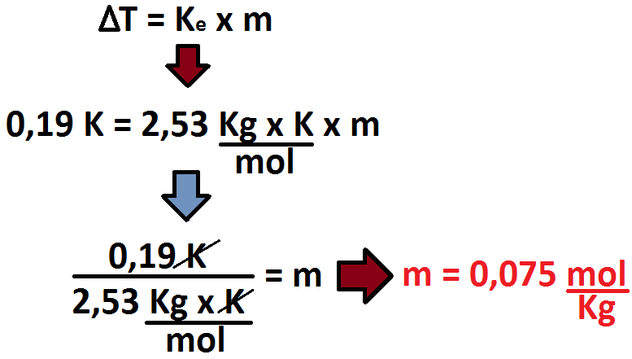
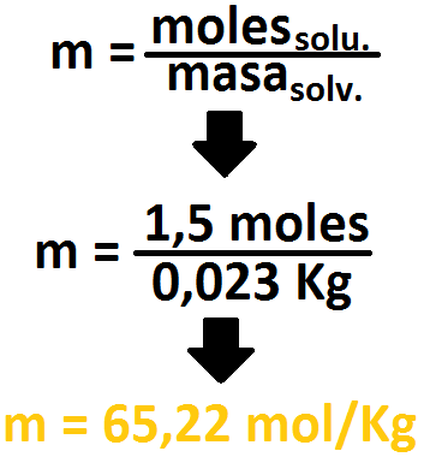
En este problema se nos exige determinar la diferencia que sufrió el punto de ebullición cuando se formó una solución. En los datos tenemos todo lo necesario para poder calcular la molalidad, y con eso, posteriormente, calcular la interrogante propuesta (recordar que
i = 1, por lo que la omitiremos):
.
11.
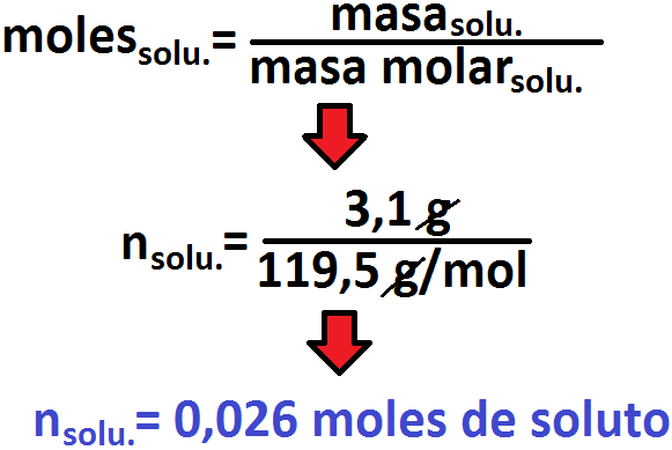
Este ejercicio tiene unas ciertas pillerías en el enunciado que deben ser idetificadas rápidamente para evitar cualquier error. Primero, identificamos lo que se nos pregunta (en este caso, la constate crioscópica, Kc). para calcular la incógnita debemos tener la molalidad y la diferencia en el punto de fusión (cuyo valor viene dado en el enunciado). Primero calculemos la molalidad:
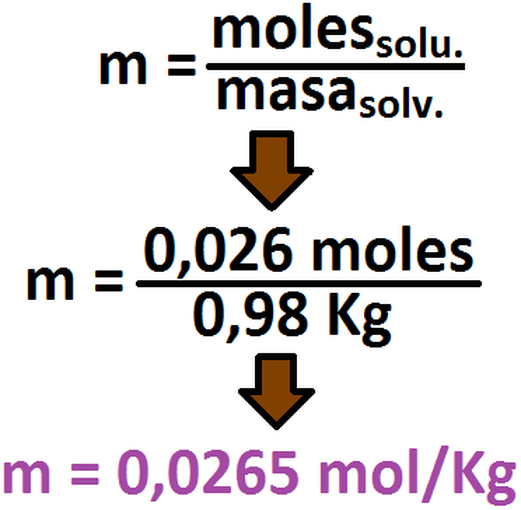
Ahora bien, con un simple cambio de unidad y aproximando, diremos que 984,24 g = 0,98 Kg, por lo cuál tendremos lo siguiente:
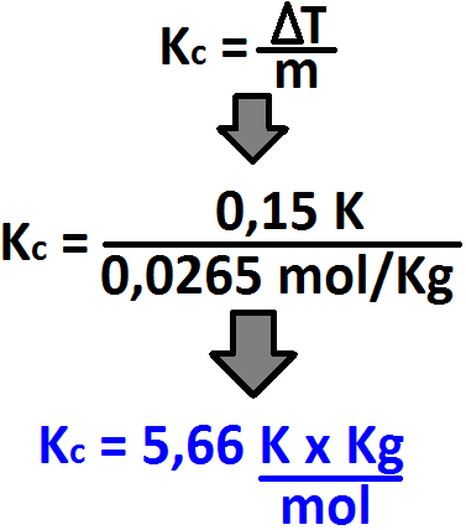
Una vez calculada la concentración molal, estamos en condiciones recién de poder calcular la constante crioscópica del solvente
recuerden que i = 1, por ende, la ecuación puede expresarse de la siguiente manera):
12.
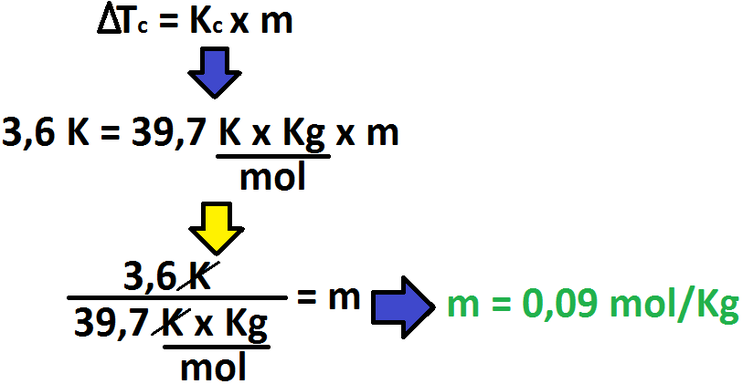
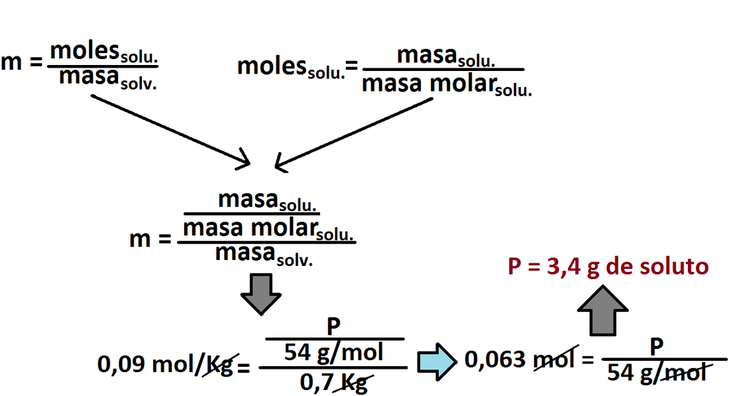
Para resolver el ejercicio, primero debemos ver en cuánto disminuyó la temperatura de congelación (o fusión) y así poder calcular la concentración molal. Con este dato podremos obtener, entonces, la masa de soluto requerida.
Como el valor de i = 1, entonces se omitirá para simplificar la expresión: