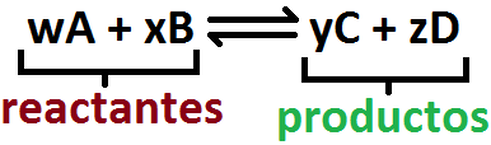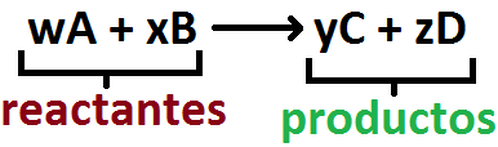Reactividad Química
Las sustancias químicas tienden a reaccionar unas con otras para formar sustancias nuevas y distintas a las iniciales. A este proceso se le llama reacción química, y se puede clasificar en dos grupos principales: reacciones reversibles y reacciones irreversibles.
El primer grupo de reacciones corresponde a todas aquellas reacciones químicas en donde las sustancias iniciales (reactantes) forman sustancias nuevas (productos), pero a su vez los productos se unen nuevamente para volver a generar los reactantes, formándose lo que se conoce como equilibrio químico (se representa con dos flechas, una de izquierda a derecha y la otra a la inversa, ver Imagen RQ-1.Por su parte, una reacción irreversible es aquella en donde los reactantes forman productos de manera total, es decir, éstos últimos no tienen la posibilidad de volver a generar los reactantes (se representa con una flecha que va de izquierda a derecha, Imagen RQ-2.
Imagen RQ-1: Reacción reversible
Imagen RQ-2: Reacción irreversible
La manera en que se anotaron las reacciones en las imágenes precedentes se denomina ecuación química,y como toda ecuación, representa una igualdad. Los reactivos siempre se anotan al costado izquierdo de la igualdad (de la flecha), mientras que los productos siempre se anotan en el costado derecho. Las letras w, x, y, z que aparecen arriba corresponden a los factores estequiométricos (para mayor información sobre factores estequimétricos vean el anexo sobre estequiometría). En una reacción química, tanto antes como después de ella, debe mantenerse la masa y la carga total del sistema.
Existen diferentes tipos de reacciones químicas: ácido-base, REDOX, de complejación y de precipitación (entre las más importantes), las cuales serán vistas en esta página.
Vídeo relacionado: