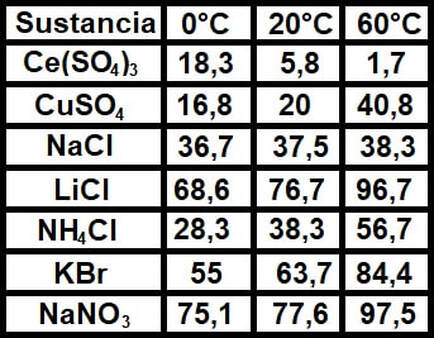
Tabla de solubilidades a diversas temperaturas
Las unidades de esta tabla son g de soluto/100mL de agua.
(Datos extraídos del gráfico presente en sabelotodo.org)
INFORMACIÓN RELEVANTE: FACTORES QUE AFECTAN LA SOLUBILIDAD
Algunos factores que afectan la solubilidad de alguna sustancia en un solvente determinado son principalmente: la presión, la temperatura y la naturaleza del soluto y del solvente.
La presión solamente afecta a disoluciones en donde se ven involucradas sustancias gaseosas (ya que los líquidos y sólidos son incompresibles, o sea, no se pueden comprimir). Por lo general, a medida que se aumenta la presión aumenta la solubilidad de una sustancia gaseosa en disolución, debido a que se le fuerza a meterse más en la sisolución y se le hace más facil al solvente "hacer su trabajo".
La temperatura afecta a todos los sistemas y, generalmente, a medida que se aumenta la temperatura se aumenta la solubilidad (en caso de los líquidos y sólidos) y se disminuye para el caso de los gases. Esto se debe a que las moléculas y átomos del soluto en cuestión adquieren más energía cinética (se mueven más rápido) lo que favorece la probabilidad de que puedan ser solvatados por el solvente, en caso de que el soluto sea sólido o líquido . En cambio, los gases, al tener más energía cinética sus partículas, éstas escapan de la disolución, desfavoreciendo el contacto con el solvente y, por ende, disminuyendo su solubilidad.
La naturaleza del solvente y del soluto no carece de importancia ya que si el soluto es polar, solamente se disolverá en solventes polares (como el agua o el etanol), mientras que si el soluto es apolar, solo lo hará en solventes apolares (como el hexano o el benceno). La misma situación ocurre desde el punto de vista del solvente, éste solo disolverá a los de su misma "clase" (polar disuelve a polar y apolar disuelve a apolar).
Vídeo relacionado: