Balance de ecuaciones químicas
El balance de ecuaciones químicas es un procedimiento mediante el cual se hace cumplir la Ley de Lavoisier dentro de una reacción química. Para ello, la cantidad de átomos en reactantes tiene que ser igual a la cantidad de átomos en productos, ya que no existe formación ni pérdida de éstos, sino que simplemente una recombinación, es decir, los átomos se ordenan de una manera distinta cuando se someten a una reacción química.
Existen diversos métodos de balance, y en esta sección hablaremos de dos en particular: el método al tanteo y el método algebraico. Ambos métodos tienen sus aspectos positivos y desfavorables y da lo mismo cual se escoja, ya que lo esencial es que se pueda lograr un balance de ecuación química correcto (ya que de otra manera, todo lo que hagamos respecto a una reacción química no será correcto).
Método al tanteo:
El método al tanteo también es conocido como el método de inspección, ya que su forma de proceder se basa en la inspección visual de la ecuación y, mediante ensayo y error, llegar a la combinación correcta de coeficientes estequiométricos. Este método es relativamente fácil de aprender y de rápida ejecución, pero existe una mayor probabilidad de error o de quedarse estancado, sobre todo con ecuaciones que puedan resultar más complejas. Si pudiésemos crear un paso a paso de este método sería como sigue:
- Igualar todos aquellos átomos que sean distintos de oxígeno e hidrógeno.
- Igualar los átomos de oxígeno.
- Igualar los átomos de hidrógeno.
- Verificar que todo esté correctamente balanceado, en caso de que no, modificar los coeficientes estequiométricos hasta corregir el error.
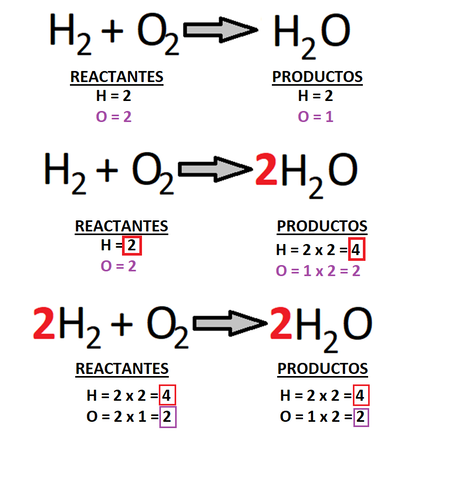
En la imagen E-BQ-1 se da un ejemplo de balance por método al tanteo de la reacción de formación del agua.
Imagen E-BQ-1: Reacción de formación del agua (balanceada mediante método al tanteo)
Como puede apreciarse, en la reacción precedente solo tenemos átomos de hidrógeno y oxígeno, por lo que el primer punto no se aplica. Luego, se equilibraron los átomos de oxígeno (al color un coeficiente estequiométrico, este se multiplica con los sub-índices de cada elemento dentro de una fórmula química, por lo que al poner el 2 delante de la molécula de agua, no solo multiplica al sub-índice 1 del oxígeno, sino que también lo hace con el 2 del hidrógeno). Posteriormente se igualan los hidrógenos, anteponiendo un 2 frente a la molécula de H2; para finalmente verificar que el balance se realizó de manera correcta.
Método algebraico:
Por su parte, el método algebraico se basa en un procedimiento matemático sistemático, con una serie de pasos claramente definidos, lo que propicia llegar a una respuesta correcta con seguridad. Sin embargo, es un procedimiento algo más engorroso y donde la persona debe tener una buena base matemática para desarrollarlo, por lo que es el método que, generalmente, cuesta más en aprender.
Los pasos de este método son:
- Visualizar los coeficientes estequiométricos con letras o símbolos (todos deben ser distintos entre sí, e idealmente, que no sean iguales a los símbolos químicos de los elementos involucrados en la reacción, para así evitar confusiones).
- Determinar cuánto de cada elemento hay en reactantes y en productos (recuerda que estos términos deben incluir la letra o símbolo que determinaste en el paso anterior).
- Igualar los elementos de misma naturaleza
- Asignar a la letra que más veces se repita el valor de 1
- Determinar el valor de las otras letras (en caso de que haya una fracción, todas las letras han de multiplicarse por el mínimo común múltiplo entre todos los denominadores).
- Verificar que la ecuación esté correctamente balanceada (así te cercioras que no hubo algún error matemático durante el proceso).
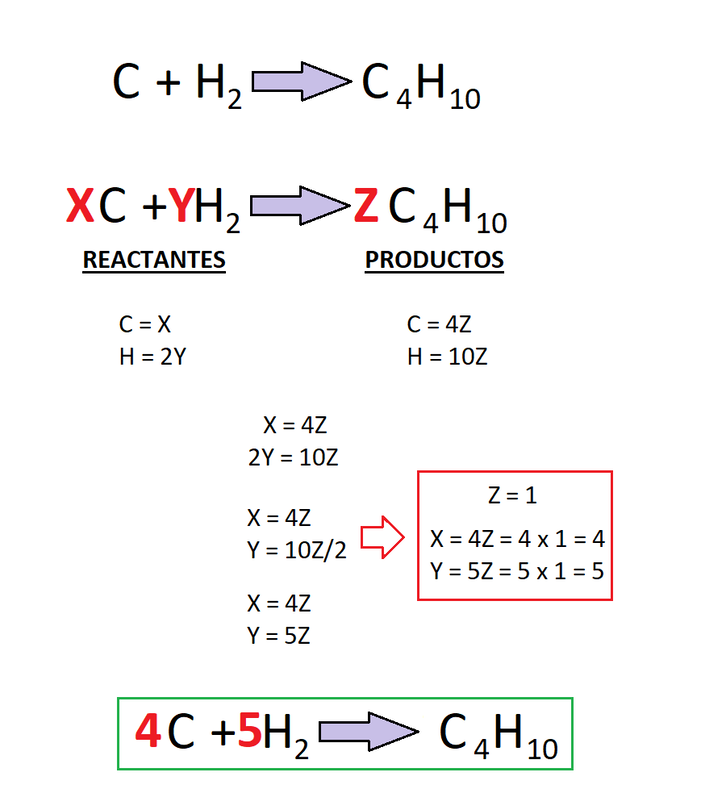
Todo esto aparece resumido en la imagen E-BQ-2.
Imagen E-BQ-2: Reacción de formación del butano (balanceado por método algebraico)
Sin importar el método que se escoja, es importante que se logre un balance de ecuación química de manera correcta, para así poder desarrollar los cálculos que continúan de manera correcta.
Vídeos relacionados:
|
|
|