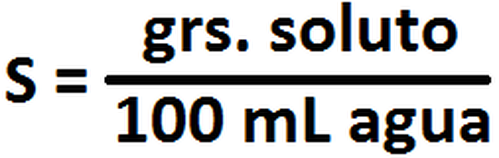Reacciones de Precipitación y Solubilidad
Tal como se vio con anterioridad, para crear una solución necesitamos que un soluto se solvate (o disuelva) en un solvente, y, vimos también, alguno de los factores que afectaban la solubilidad de un soluto en un solvente determinado. Sin embargo, en esta sección profundizaremos más sobre el término de solubilidad, e introduciremos nueva terminología como Kps (constante de solubilidad).
Partamos primero por definir bien lo que es solubilidad. Según Sokolsky (en "Remington: Famacia", p. 243 (2003)), la solubilidad puede definirse como el grado en el que se disuelve un soluto en un solvente a una temperatura determinada (temperatura del experimento), es decir, a medida que crece la solubilidad, mayor es la cantidad de soluto que puede disolverse en dicho solvente, manteniendo la temperatura constante. Este último dato es sumamente importante, ya que, como vimos antes, la temperatura afecta la solubilidad.
Teniendo esto como base de análisis, podemos entonces clasificar a las soluciones en tres categorías distintas, según la relación entre lo que está disuelto y su solubilidad:
- Insaturada: Es toda aquella solución en donde la cantidad de soluto presente en ella es menor que su solubilidad.
- Saturada: Es aquella en donde la cantidad de soluto presente en ella es igual a su solubilidad.
- Sobresaturada: Es aquella solución en donde la cantidad de soluto presente en ella es mayor a su solubilidad. En este caso, empieza a originarse el fenómeno denominado precipitación.
La solubilidad se calcula por lo general (para soluciones acuosas) a partir de la ecuación contenida en la Imagen RQP-1:
Imagen RQP-1: Cálculo de solubilidad en disoluciones acuosas (obtenido de Correa, C. <<Fenómenos Químicos>> (159). Medellín: Ed. Universidad EAFIT, 2004).
Es así entonces que cada especie química tendrá una solubilidad diferente cuando se mezcla con un mismo solvente (por ejemplo, en el Anexo 2 pueden hallar una tabla de solubilidades de diversas sustancias en solución acuosa, a diversas temperaturas). Es por este motivo que se utiliza esta propiedad para poder realizar identificaciones y separaciones mediante gravimetría, es decir, mediante la formación de un sólido que caiga (precipite) al fondo del recipiente donde ha ocurrido la reacción para, posteriormente, realizar los cálculos según la masa obtenida de dicho sólido (denominado "precipitado").
Para realizar esto, se requiere que las sustancias que se han de separar presenten Kps suficientemente distintos entre sí (mínimo 100 veces menor una de otra), ya que de caso contrario, ambas especies precipitarán conjuntamente y no habrá servido de nada realizar la gravimetría. En relación a esto, es importante recordar que siempre precipitará primero el que presente una menor constante de solubilidad, por lo que se puede decir que a menor constante de solubilidad, menos soluble es la especie (o más insoluble).