Electropositividad y Energía de Ionización
Para finalizar, analizaremos muy brevemente lo que es la electropositividad y el potencial de ionización.
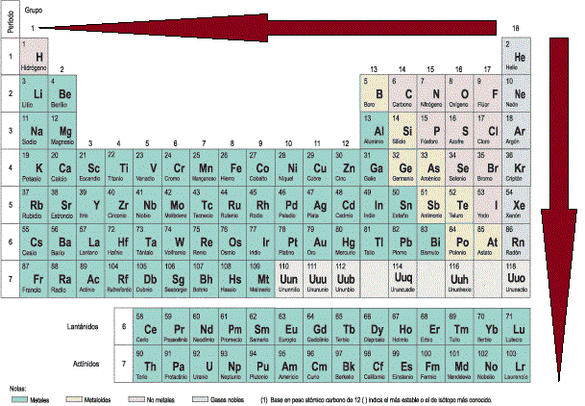
Imagen PPP-1: Direcciones de crecimiento de la electropositividad en la Tabla Periódica.
- Electropositividad: La electropositividad es lo contrario a la electronegatividad es decir, es la capacidad de un elemento de ceder electrones o densidad electrónica y por lo tanto, crece en direcciones contrarias a su opuesto, es decir, aumenta al bajar por un grupo y disminuye al avanzar en un período (Imagen PPP-1). Si bien, mirando la tabla periódica, se diría que el Francio (Fr) es el elemento más electropositivo, se considera por lo general al Cesio (Cs) como tal, debido a que el Francio es radiactivo y se descompone fácilmente en otros elementos.
Imagen PPP-1: Direcciones de crecimiento de la electropositividad en la Tabla Periódica.
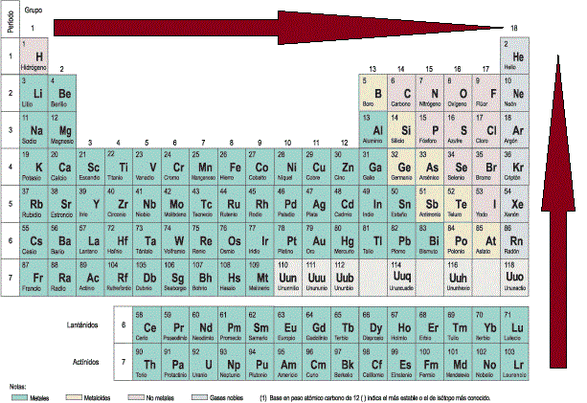
- Potencial de Ionización: El potencial (o energía) de ionización corresponde a la energía necesaria que se debe administrar a un elemento para que ceda su electrón más externo. Cada elemento polielectrónico tiene tantos potenciales de ionización como electrones tenga, siendo siempre el primer potencial el menor de todos y va aumentando a medida que se van quitando los electrones, es decir, se va haciendo cada vez más difícil extraer los electrones que están más cerca del núcleo que los que están más alejados de éste. Como un aumento de energía implica dificultad, los no-metales (ubicados al costado derecho de la tabla periódica) poseen las energías más altas, por lo cual el potencial de ionización aumenta a medida que se avanza en un periodo; mientras que a medida que un átomo se hace más grande es más sencillo extraer su electrón más alejado, ya que este se siente menos atraído hacia el núcleo (revise las secciones correspondiente a radio atómico y radio iónico y a electronegatividad y electroafinidad), por lo cual la energía de ionización disminuye a medida que se baja en un grupo, todo esto se ve resumido en la Imagen PPP-2.
Imagen PPP-2: Direcciones de crecimiento de la Energía de Ionización en la Tabla Periódica.
Con esto se concluye este capítulo sobre las propiedades periódicas, las que nos darán una base para poder explicar los enlaces químicos existentes (tema del próximo capítulo).