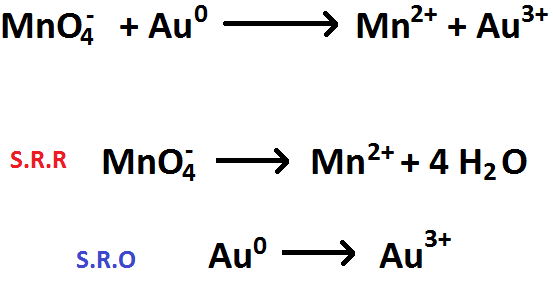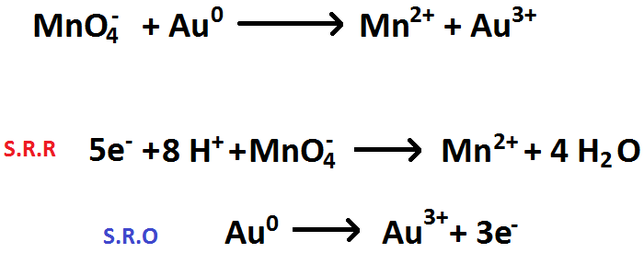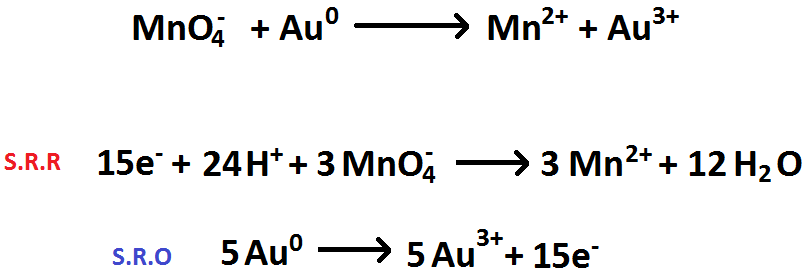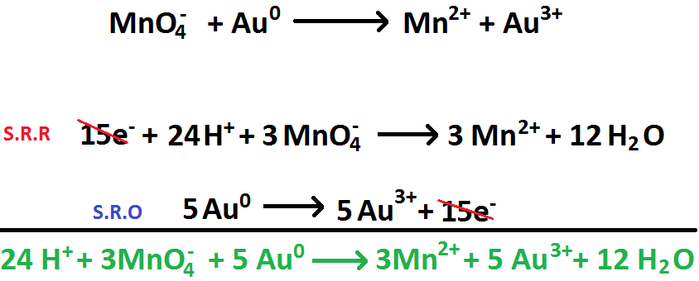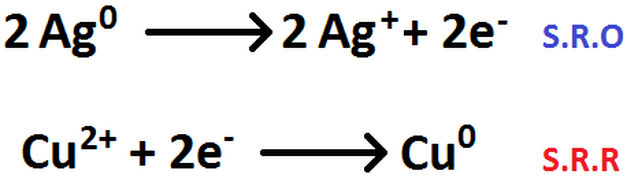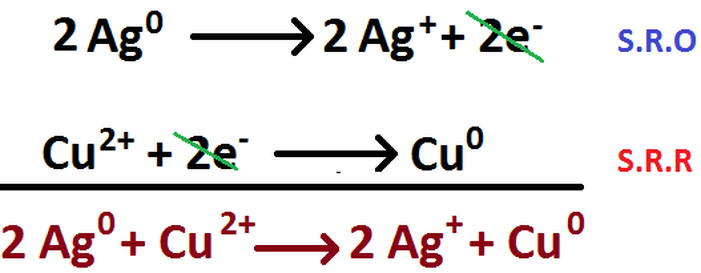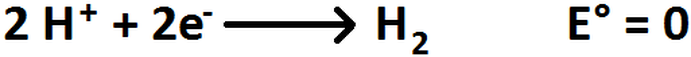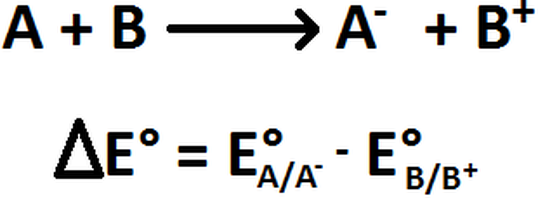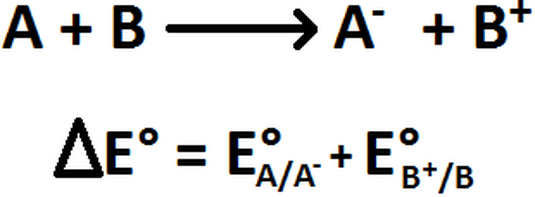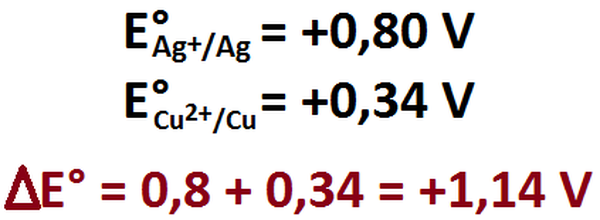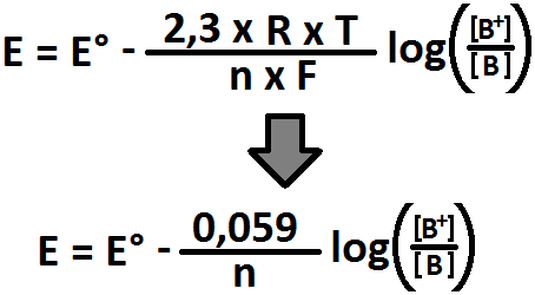Reacciones REDOX
La palabra REDOX es una sigla de óxido-reducción (en inglés, reduction-oxidation), lo cuál resume este tipo de reacciones: una sustancia se oxida y otra se reduce. Por lo general, a la sustancia que se oxida se le denomina agente reductor (debido a que provoca la reducción de la otra sustancia), mientras que a la sustancia que se reduce se le llama agente oxidante (provoca la oxidación de la otra sustancia). Pero, ¿en que consiste este tipo de reacciones? Una reacción REDOX consiste en el traspaso de electrones desde una sustancia X (agente reductor) hacia una sustancia Y (agente oxidante). Una aplicación en la vida cotidiana de este tipo de reacciones son las pilas que usamos a dierio en varios aparatps, como despertadores, calculadoras, relojes, celulares, etc..
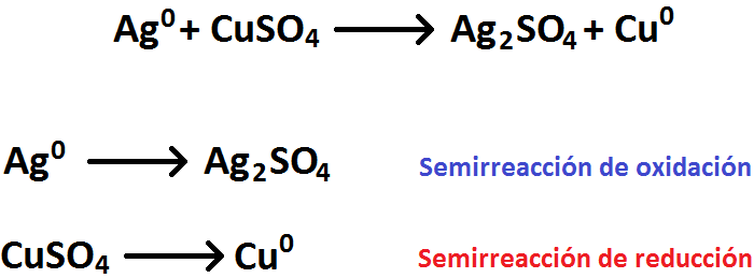
Cabe destacar que en este tipo de reacciones, tanto la oxidación como la reduicción ocurren de manera simultánea (al mismo tiempo). A pesar de eso, la manera en la que se equilibria su ecuación química separa ambas situaciones, formándose lo que se denoiminan las semirreacciones (de oxidación y reducción, respectivamente). En la primera, se anotan todas las sustancias involucradas en la oxidación, es decir, en la parte donde debiesen ir los reactantes se anota la especie que se va a oxidar, mientras que en lado de los productos se anota la especie ya oxidada. Análogamente, se hace una cosa similar para la semirreacción de reducción (S.R.R). Todo esto se ve en la Imagen RQR-1, que muestra el ejemplo de la reacción entre Ag y CuSO4.
Imagen RQR-1: Reacción entre Ag y CuSO4.
Pero, ¿qué significa ese cero sobre el símbolo de la Plata (en reactantes) y del Cobre (en productos)? Para contestar esta pregunta, debemos tener en cuenta el término de Estado de Oxidación (E.O). El Estado de Oxidación es un número irreal (no existe realmente, sino que es una creación humana para poder facilitar el estudio de este tipo de reacciones) que nos indica la tendencia de dicho elemento a captar electrones. Cada número de E.O va acompañado de un signo: si el elemento acepta electrones adquiere un signo menos (-), mientras que si cede, adquiere un signo positivo (+). Existen ciertas reglas que nos ayudan a conocer el E.O de todos los elementos de la tabla periódica, las cuáles son:
- Si un elemento se encuentra en su estado fundamental, su E.O es igual a cero (0).
- El Oxígeno presenta E.O igual a -2 en todos los compuestos que forma, salvo en los Peróxidos donde su E.O es -1.
- El Hidrógeno presenta un E.O igual a +1 en todos sus compuestos, salvo en los Hidruros Metálicos, donde su E.O es -1.
- Los cationes y aniones presentan un E.O igual a su carga.
- Si un Compuesto es neutro eléctricamente, entonces la suma de los E.O de sus elementos constituyentes es igual a 0.
- Si un Compuesto esta cargado eléctricamente, entonces la suma de los E.O de sus elementos constituyentes es igual a la carga.
Con esto, podríamos decir que si una especie aumenta su Estado de Oxidación, dicha especie se oxidó; mientras que si una sustancia disminuye su E.O, entonces se redujo. También cabe hacer notar que cuando un elemento presenta E.O = 0, se le coloca un 0 sobre su símbolo químico, tal y como lo que pasó con la Plata y el Cobre, en nuestro ejemplo anterior; y que si existe más de un elemento en un mismo compuesto, el E.O de dicho elemento se multiplica tantas veces como átomos hayan del elemento, por ejemplo, en el ácido sulfúrico (H2SO4) existen 2 Hidrógenos y 4 Oxígenos, por lo cual, para calcular el E.O del azufre , la ecuación matemática nos quedaría:
2 x H + S + 4 x O = 0
2 x (+1) + S + 4 x (-2) = 0
2 + S - 8 = 0
S - 6 = 0
S = +6
2 x (+1) + S + 4 x (-2) = 0
2 + S - 8 = 0
S - 6 = 0
S = +6
Volviendo al ejemplo de la Imagen 52, nosotros podríamos simplificar la semirreción de oxidación (S.R.O) y la semirreacción de reducción (S.R.R) eliminando los contraiones (en este caso, el ión sulfato), ya que no aportan nada para el equilibrio de la ecuación. Por ende, dichas semirreacciones me quedarían tal y como aparecen en la Imagen RQR-2.
Imagen RQR-2: Semirreacciones del ejemplo anterior.
Existen distintas formas para equilibrar estas semirreacciones. La que veremos aquí se denomina método del ión-electrón y se ocupa en medio ácido, sin embargo, usaremos un truco para poder equilibrar la ecuación general en medio básico. Para equilibrar la ecuación según este método debe seguirse los pasos siguientes:
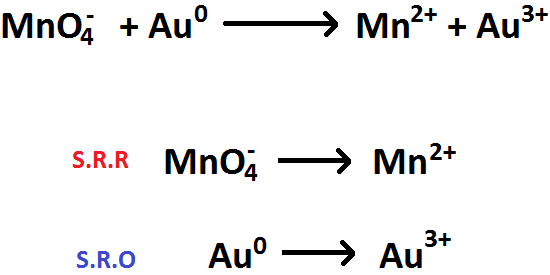
1. Se igualan los átomos centrales (cuando sea sea necesario) en ambos extremos de la semirreacción (Imagen RQR-3)
Imagen RQR-3: Ejemplo del paso 1. para equilibrar reacciones REDOX.
2. Si una sustancia presenta exceso de Oxígenos en relación a la otra, se añaden tantas moléculas de agua como oxígenos
sobrantes hayan (Imagen RQR-4).
Imagen RQR-4: Ejemplo del paso 2. para equilibrar reacciones REDOX.
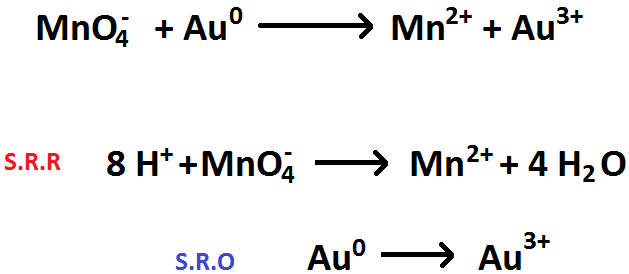
3. Si a un costado de la semirreacción existe un exceso de Hidrógenos, al otro costado se agregarán tantos protones como exceso de
H exista (Imagen RQR-5).
Imagen RQR-5: Ejemplo del paso 3. para equilibrar reacciones REDOX.
4. Si existe un exceso de cargas positivas en un lado de la semirreacción, se agregarán electrones a ese lado de tal manera
que la carga neta sea igual en ambos extremos (Imagen RQR-6).
Imagen RQR-6: Ejemplo del paso 4. para equilibrar reacciones REDOX.
5. Se igualan los electrones en ambas semirreacciones multiplicándolas por lo que sea necesario para lograr esa igualdad (en la
Imagen RQR-7 la S.R.R se multiplicó por 3 y la S.R.O se multiplicó por 5).
Imagen RQR-7: Ejemplo del paso 5. para equilibrar reacciones REDOX.
6. Finalmente se suman ambas semirreacciones de la siguiente manera: todo aquello que se encuentre a un mismo lado de la
semirreacción se suma, mientras que lo que se encuentre al lado opuesto se resta (debido a eso se cancelan los electrones).
Todo esto se ve en la Imagen RQR-8.
Imagen RQR-8: Ejemplo del paso 6. para equilibrar reacciones REDOX.
De esta manera se equilibran las ecuaciones REDOX (en medio ácido). Ahora aplicaremos esto para el ejemplo inicial que teníamos (la reacción entre la Plata y el Sulfato de Cobre), por lo que las semirreacciones nos quedarían tal y como se muestran en la Imagen RQR-9.
Imagen RQR-9: Semirreacciones equilibradas del ejemplo de la Imagen 52.
Y por último, sumando ambas semirreacciones nos quedaria lo que se muestra en la Imagen RQR-10.
Imagen RQR-10: Resultado final del ejemplo de la Imagen 52.
Ahora bien, ¿cómo podemos saber que especie va a tender a oxidarse y cual a reducirse? Para eso se ocupa lo que se llama los potenciales de reducción estándar (E°), los cuales toman como referencia la reducción de 2 protones a hidrógeno gaseoso, tal y como se muestra en la Imagen RQR-11.
Imagen RQR-11: Semirreacción de reducción para el Hidrógeno.
Como son potenciales, todos ellos se miden en Volts (V), la misma unidad que se usa para el voltaje de nuestras casas. A partir de este potencial se van sacando los otros, siendo números positivos todas aquellas sustancias que tiendan a reducirse y poseen un potencial negativo todas las sustancias que no tiendan a reducirse (es decir, que tiendan a oxidarse). Es así entonces como uno puede comparar dos sustancias y ver quien se oxidará y quien se reducirá.
Se puede calcular también la diferencia de potencial (o voltaje) de reducción de la reacción general con la fórmula que aparece en la Imagen RQR-12.
Imagen RQR-12: Cálculo del Voltaje de reducción de una reacción.
Siendo E°A/A- el potencial de reducción de la especie que se reduce y E°B/B+ el potencial de oxidación de la especie que se oxida. Esta diferencia de potencial siempre es un número positivo (si fuera negativo, entonces se dice que la reacción no ocurre en el sentido en el que está escrito). El de potencial de oxidación es análogo al de reducción, ya que su valor es igual al potencial de reducción pero con signo cambiado (por ejemplo, si el potencial de reducción de una sustancia X era +0,7; su potencial de oxidación será de -0,7). Sin embargo, en esta página web, nosotros hablaremos de manera casi exclusiva de los potenciales de reducción, que es lo que se usa para los cálculos. De esa manera, al ecuación de la imagen anterior se transforma en la de la Imagen RQR-13.
Si todo esto lo aplicamos a nuestro ejemplo anterior (Imagen RQR-1) entonces podríamos calcular su diferencia de potencial (Imagen RQR-14).
Imagen RQR-13: Cálculo de la diferencia de potencial de una reacción usando solo potenciales de reducción.
Imagen RQR-14: Diferencia de potencial para el ejemplo de la Imagen 52.
Sin embargo, estos valores fueron tomados para cuando la concentración era 1 mol/L y la presión era de 1 atm a 25°C. Si se desea trabajar a condiciones distintas, ya no es factible usar los potenciales de reducción estándar (E°), sino que simplemente ahora pasan a ser potenciales de reducción (E) y la manera de calcularlos es a través de la ecuación de Nernst (Imagen RQR-15), la cuál muestra claramente que los potenciales dependen tanto de la temperatura como de la concentración.
Imagen RQR-15: Ecuación de Nernst.
En donde n es el número de electrones transferidos en la semirreacción, T es la temperatura en Kelvin (K = 273,15 + °C), R la constante de los gases ideales (8,31 J/(mol x K)) y F es la constante de Faraday (96.485,31 C/mol), [B] es la concentración (molar) de la especie reducida y [B+] es la concentración (molar) de la especie oxidada. Cabe hacer notar que la ecuación (2,3 x R x T) / F = 0,059 es válido exclusivamente para cuando T = 25°C (ó 298,15 K), si se trabaja a otras temperaturas se tiene que usar la expresión superior.