Teoría Ácido-Base de Lewis
Gilbert Lewis, científico estadounidense, planteó una teoría ácido-base basándose en las estructuras propuestas por él mismo (ver Anexo 1) a inicios del siglo XX. Según Lewis, un ácido era una sustancia química capaz de aceptar un par electrónico, completando así su octeto y por ende logrando estabilidad, mientras que una base era una sustancia química que poseía a lo menos un par electrónico libre (sin enlazar). Como se puede ver, este tipo de definición necesita obligatoriamente un par ácido-base actuando en conjunto, debido a que, por lo general, es imposible dejar electrones libres en un medio cualquiera (salvo con nitrógeno líquido). Una imagen que represente este tipo de enlace se ve en la Imagen 33, donde se puede apreciar claramente que uno de los dos pares electrónicos del oxígeno se comparte con un ion hidrógeno.
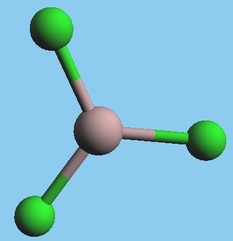
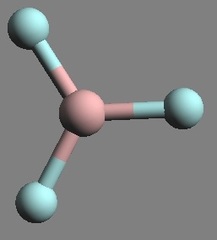
Por lo general, los ácidos de Lewis corresponden a metales (sobre todo a metales de transición), a cationes, y a compuestos con aluminio o boro (como los que se ven en la Imagen DAL-1(a) y en la Imagen DAL-1(b)). Por su parte, las bases de Lewis corresponden principalmente a aniones, no-metales (sobre todo los de los grupos 15, 16 y 17) y sus derivados (como el ion hidroxílo mostrado en la Imagen DAA-2, en donde la parte básica está localizada en el oxígeno).
Imagen DAL-1: Vista de dos ácidos de Lewis: a) Compuesto de Aluminio; b) Compuesto de Boro.
Ahora, pasaremos a ver lo que pasa cuando una base y un ácido se juntan en una disolución (el término disolución se verá en el próximo capítulo). Además, en la proxima sección se verá como identificar un ácido y una base fuerte de una débil, respectivamente.