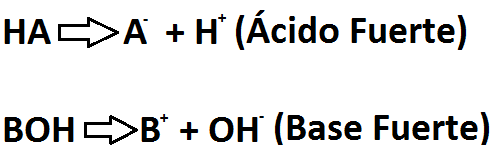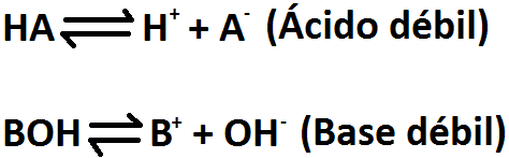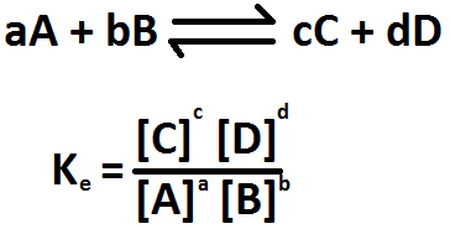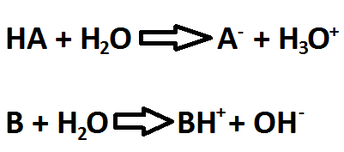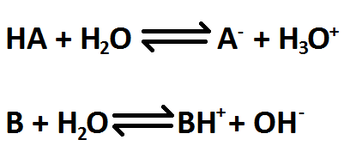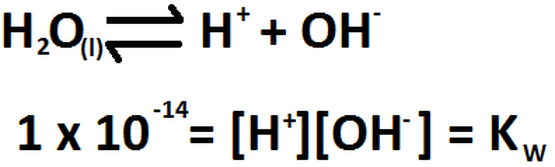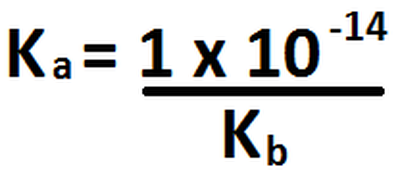Reacciones entre un ácido y una base
Cada rama de la química prefiere usar alguna de las diferentes definiciones ácido-base con las que se disponen, por ejemplo, en Química Analítica Inorgánica se suele usar la teoría de Lowry para explicar los fenómenos que ahí se estudian; mientras que, en Química Orgánica, la teoría de Lewis es la más utilizada para explicar muchas de las reacciones ácido-base que involucran reactivos orgánicos.
En esta sección nos enfocaremos a lo que corresponde a Química Analítica (inorgánica), por lo cual, mayormente utilizaremos la teoría de Lowry, aunque también será útil, para ciertos reactivos, utilizar la de Arrhenius. Pero antes de ver como se producen este tipo de reacciones químicas, es necesario introducir una nueva clasificación: los ácidos/bases fuertes y los ácidos/bases débiles.
Se dice que un ácido o una base es fuerte (ver Imagen RQA-1) cuando al entrar en contacto con agua se disocia completamente en sus iones formadores. Por su parte, cuando se dice que un ácido o una base es débil (ver Imagen RQA-2), quiere decir que no se disocia por completo en agua, por lo cual es posible encontrar tanto al ácido o a la base en forma disociada, como también en su forma molecular. Cuando una sustancia tiene este comportamiento (cuando se disocia en iones) se dice que dicha sustancia es un electrolito (sustancia capaz de transmitir una corriente eléctrica), por lo cuál los ácidos/bases fuertes son electrolitos fuertes, mientras que los ácidos/bases débiles son electrolitos débiles.
Imagen RQA-1: Generalización de un ácido y una base fuerte
En esta sección nos enfocaremos a lo que corresponde a Química Analítica (inorgánica), por lo cual, mayormente utilizaremos la teoría de Lowry, aunque también será útil, para ciertos reactivos, utilizar la de Arrhenius. Pero antes de ver como se producen este tipo de reacciones químicas, es necesario introducir una nueva clasificación: los ácidos/bases fuertes y los ácidos/bases débiles.
Se dice que un ácido o una base es fuerte (ver Imagen RQA-1) cuando al entrar en contacto con agua se disocia completamente en sus iones formadores. Por su parte, cuando se dice que un ácido o una base es débil (ver Imagen RQA-2), quiere decir que no se disocia por completo en agua, por lo cual es posible encontrar tanto al ácido o a la base en forma disociada, como también en su forma molecular. Cuando una sustancia tiene este comportamiento (cuando se disocia en iones) se dice que dicha sustancia es un electrolito (sustancia capaz de transmitir una corriente eléctrica), por lo cuál los ácidos/bases fuertes son electrolitos fuertes, mientras que los ácidos/bases débiles son electrolitos débiles.
Imagen RQA-1: Generalización de un ácido y una base fuerte
Imagen RQA-2: Generalización de un ácido y una base débil.
Pero ahora, ¿cómo se pueden distinguir ácidos o bases fuertes de débiles? Bueno, eso dependerá del tipo de ácido y base que estemos analizando. Si es un ácido binario (compuesto por dos elementos), se deben aprender no más, ya que son pocos, estos son: HCl, HBr y HI (el HF es débil, a pesar de pertencer al mismo grupo del Cl, Br, e I). Ahora si estamos analizando un ácido ternario (compuesto por tres elementos), una forma práctica de ver cuál es fuerte y cual no es realzar esta simple ecuación:
F = Nro O - Nro H
Siendo F = fuerza del ácido, Nro O = número de átomos de oxígeno presentes y Nro H = número de átomos de Hidrógenos presentes. Ahora si F es menor a 2, el ácido es débil; mientras que si F es mayor o igual a 2 el ácido se considerará fuerte. Teniendo en consideración podemos decir por ejemplo que:
- HNO2 = Débil. (2 - 1 = 1)
- HNO3 = Fuerte. (3 - 1 = 2)
- HClO = Débil. (1 - 1 = 0)
- HClO4 = Fuerte. (4 - 1 = 3)
Para poder identificar las bases fuertes es mucho más sencillo, ya que entrarán en esta categoría las bases hidroxiladas (como el NaOH o el KOH, entre otras). Si bien, existen otras bases fuertes en otras ramas de la química (como en química orgánica), nosotros por ahora solo trabajaremos con las bases hidroxiladas como fuertes y las demás se considerarán débiles (como el amoniaco).
Ahora bien, teniendo en cuanta lo anterior nos será más sencillo comprender lo que es la neutralización entre un ácido y una base. La palabra Neutralización se puede interpretar como aniquilación o como eliminación, lo cuál no está muy lejano a la realidad. Cuando un ácido se junta con una base, ambas especies se "aniquilan" mutuamente en diferente grados. Como en todas las cosas, los fuertes vencen a los débiles y es así que cuando, por ejemplo, un ácido fuerte se mezcla con una base débil, esta última será "eliminada" completamente, mientras que permanecerá en disolcuión el ácido fuerte. Es así que se pueden generar cuatro situaciones cuando uno mezcla un ácido con una base:
- Se mezcla un ácido Fuerte con una base Fuerte: Cuando esto sucede, la especie que quedará en disolución será la que esté en mayor cantidad respecto de la otra.
- Se mezcla un ácido Fuerte con una base Débil: La disolución generada sera del tipo ácido, ya que será el ácido el que quede en la mezcla.
- Se mezcla un ácido Débil con una base Fuerte: La disolución será básica, ya que sera la base la que permanezca en la mezcla.
- Se mezcla un ácido Débil con una base Débil: Si esto sucede, la acidez de una disolución dependera de la constante de ácidez del ácido débil y de las concentraciones tanto de la base como del ácido.
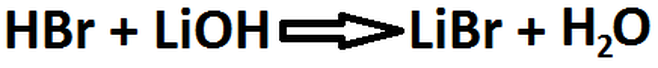
Cuando sucede cualquiera delas tres primeras sietuaciones, la reacción que se produce es irreversible (se denota por una flecha unidireccional), esto quiere decir que todos los reactantes pasan a formar productos de manera estequiométrica. El resultado de esta reacción es agua y sal (ver la Imagen RQA-3).
Imagen RQA-3: Reacción entre un ácido fuerte (HBr) y una base fuerte (LiOH).
Ahora bien, si nos encontramos en la última situación, es decir, si mezclamos un ácido débil con una base débil, la reacción será de tipo reversible (se denota por dos flechas, o semi-flechas, en sentido opuestos la una de la otra), formándose lo que se conoce como un equilibrio químico. Un equilibrio químico se produce cuando las velocidades a la que los reactantes se unen para formar los productos (velocidad directa, flecha de izquierda a derecha) se iguala con la velocidad en que los productos se descomponen en los reactantes (velocidad inversa, flecha de derecha a izquierda). En el instante en el que se produce un equilibrio químico, se pueden relacionar las especies participantes (reactantes y productos) a través de lo que se conoce como la constante de equilibrio (Ke o Keq). En esta constante NUNCA se colocan las sustancias que se encuentren en estado líquido (como el agua) ni en estado sólido. La forma de la constante para cualquier reacción se muestra en la Imagen RQA-4. Un dato importante es que cuando ocurre este tipo de reacción (entre un ácido débil y una base débil), se forma lo que se conoce como los pares ácido/base conjugada y base/ácido conjugado. Es decir, el ácido débil, después de que ocurre la reacción directa, forma una base débil llamada base conjugada. Lo mismo sucede con la base d´pebil reaccionante (forma un ácido débil denominado ácido conjugado).
Imagen RQA-4: Forma de la constante de equilibrio para la reacción entre A y B para dar C y D (a, b, c y d son los números estequiométricos).
Relacionando esto con las definiciones dadas anteriormete para ácidos fuertes y débiles, podemos deducir que solamente los ácidos y bases débiles tendrán constante de equilibrio ¿Porqué? Esto debido a que lo que ocurre realmente se muestra en la Imagen RQA-5a (para un ácido y una base fuerte) y en la Imagen RQA-5b (para un ácido y una base débil).
Imagen RQA-5: a) Reacción de disociación de un ácido y una base fuerte; b) Reacción de disociación para un ácido y una base débil.
Cuando hablamos de la constante de equilibrio d eun ácido débil, hacemos referencia a su constante de acidez (Ka), mientras que si la constante de equilibrio corresponde a una base débil, entonces nos referimos a su constante de basicidad (Kb). En el caso del agua, ocurre una situación especial, ya que el agua puede actuar como ácido débil o bien como base débil. Una sustancia con estas características se llama sustancia anfótera. Debido a esto, el agua reacciona consigo misma formando ión hidronio (simplificado como H+) e ión hidroxilo (OH-). A esta reacción comúnmente se le denomina auto-disociación del agua y su constante de equilibrio se denomina, por lo general, constante de disociación del agua (Kw). Todo esto se ve reflejado en la Imagen RQA-6.
Imagen RQA-6: Auto-disociación del agua y su constante respectiva.
Kw siempre debe cumplirse, es decir, si llega a aumentar la cantidad de protones, debe existir una disminución en la cantidad de iones hidroxilos presente en la disolución (y viceversa), por lo tanto se pueden dar tres situaciones:
- La cantidad de protones supera la cantidad de iones hidroxilos presentes en disolución.
- La cantidad de protones es idéntica a la cantidad de iones hidroxilos en disolución.
- La cantidad de protoines es menor a la cantidad de iones hidroxilos existentes en la solución.
Si se da la primera situación, se dice que la solución es ácida, si se da la segunda se dice que la solución es neutra y si finalmente nos encontramos en la tercera situación, entonces decimos que la disolcuión es básica. Todo esto se resume en la Imágen RQA-7.
Imagen RQA-7 Relaciones entre protones e iones hidroxilos.
Ahora bien, si relacionamos la Imagen 44 con la Imagen 45, veremos que lo que aparece en la Imagen RQA-8 es lo más lógico.
Imagen RQA-8: Valor crítico que determina la acidez.
Lamentablemente, es complicado trabajar con cantidades tan pequeñas, por lo que para simplificar las cosas se utilizó el operador p el cual es igual al logaritmo negativo (en base 10) de lo que se quiere analizar (se anota como -log). De esta manera, nos queda que:
-log (1 x 10-7) = 7
Por ende, si reemplazamos lo anterior en la Imagen 46, y si consideramos que al multiplicar por -1 el signo de desigualdad se "da vuelta", nos quedará lo que aparece expresado en la Imagen RQA-9.
Imagen RQA-9: Rangos de acidez según pH.
Con estos antecedentes podemos definir el pH como medida que indica cuán ácida es una disolución. Análogamente tendremos una medida que indica cuán básica es una disolución, denominada pOH, y cuyos valores extremos se encuentran expresados en la Imagen RQA-10.
Imagen RQA-10: Rangos de basicidad según pOH.
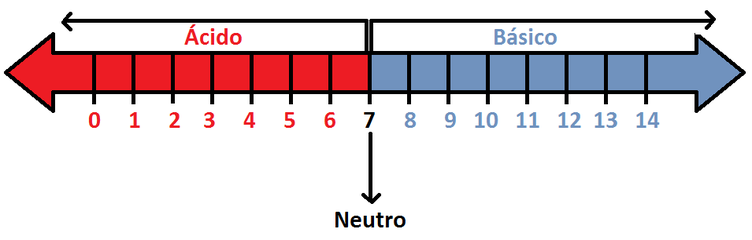
Por ende, se puede construir una escala que indique la acidez de una disolución. Dicha escala se llama escala de pH y se muestra en la Imagen RQA-11.
Imagen RQA-11: Escala de pH
La Imagen RQA-12 nos indica el resultado de aplicar el operador p a la constante Kw (ver Imagen 44). También nos entgrega una manera sencilla de calcular el pH a partir del pOH y viceversa.
Imagen RQA-12: Relación entre pH y pOH
¿Se recuerdan de lo que pasaba cuando se hacía reaccionar un ácido débil conuna base débil? Dijimos que se formaba los denominados pares ácido/base conjugada y base/ácido conjugado. Pero, si la disociación de una base débil (determinada por su Kb) genera un equilibrio y uno de sus productos es un ácido débil (ácido conjugado), entonces tambien existe un Ka en la reacción inversa (cuando los productos se unen para formar la base débil inicial). Ahora bien, si pudimos relacionar pH con pOH, ¿será posible poder relacionar el Kb y el Ka de un par base/ácido conjugado? La respuesta es SÍ y dicha relación se hace presente en la Imagen 51.
Imagen 51: Relación entre el Ka y el Kb de un par ácido/ base conjugada (es análoga para el par base/ ácido conjugado).
Nótese que la relación expuesta en la anterior es también aplicable para un par ácido/base conjugada.
Para finalizar, volveremos a las cuatros situaciones que posibles que teniamos en una neutralización, esta vez indicando el pH en el que se encontrará la disolución una vez ocurrida dicha reacción:
- Reacción entre un ácido Fuerte y una base Fuerte: Genera una disolución neutra.
- Reacción entre un ácido Fuerte y una base Débil: Genera una disolución muy ácida (valores de pH cercanos a 0).
- Reacción entre un ácdio Débil y una base Fuerte: Genera una disolución muy básica (valores de pH cercanos a 14).
- Reacción entre un ácido Débil y una base Débil: El pH de la disolución dependerá de quien sea menos débil. Si el ácido es menos débil que la base entonces la solución será débilmente ácida; mientras que si la base es menos débil que el ácido, la solución será débilmente básica. En ambos casos el pH se encontrará cercano a 7 (sin ser igual a 7).
En el Anexo 2 encontrará una tabla con los valores de los Ka de diferentes ácidos débiles que le serán de utilidad para resolver ejercicios (por lo que es probable que en el ejercicio mismo NO se le de el valor de la constante, sino que tendrá que verlo en la tabla).