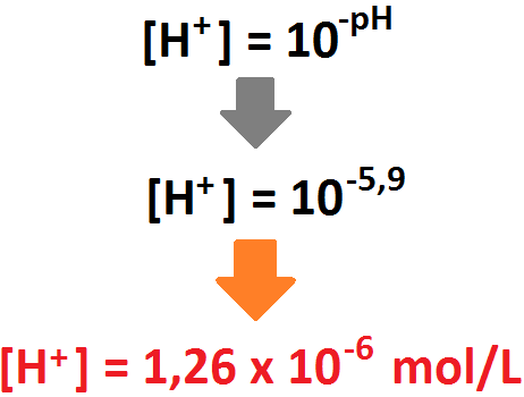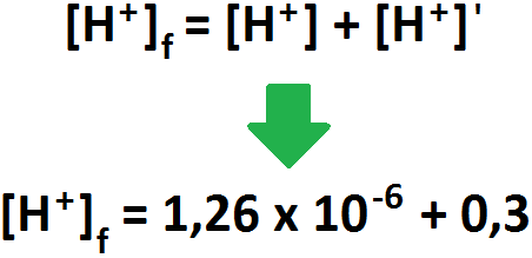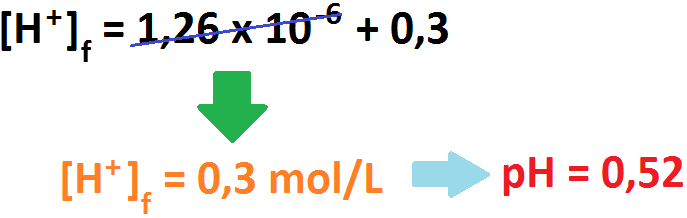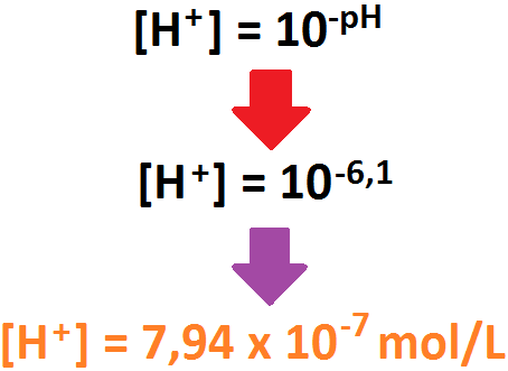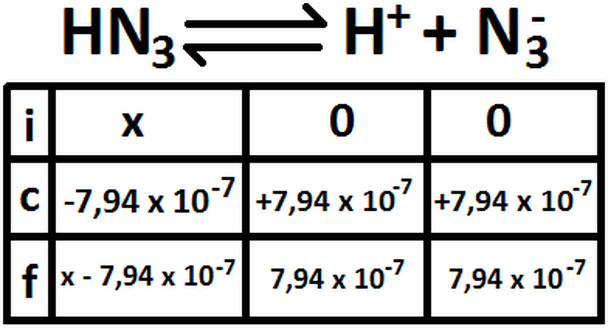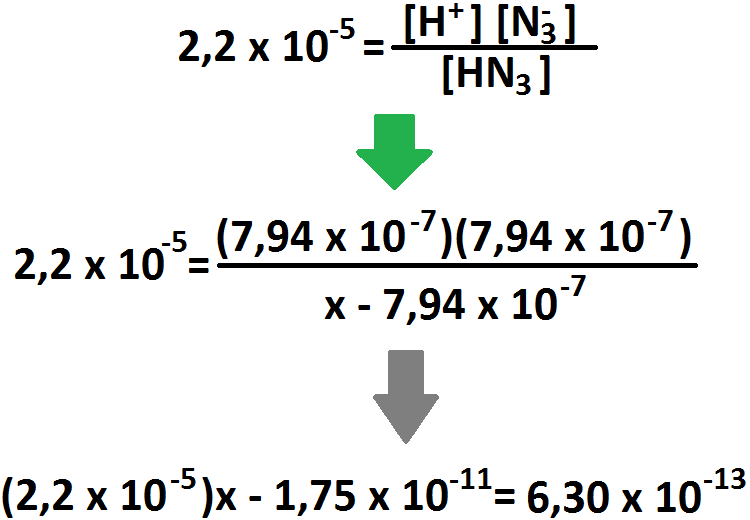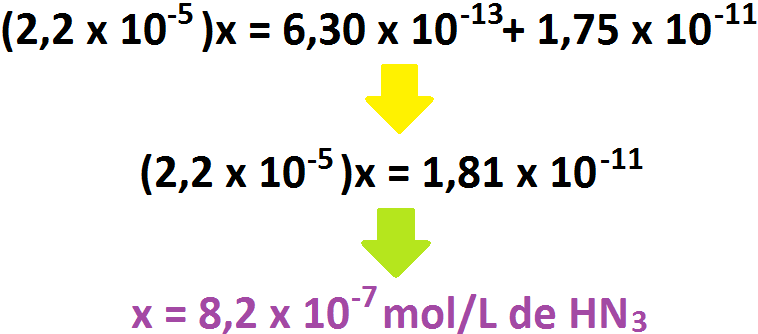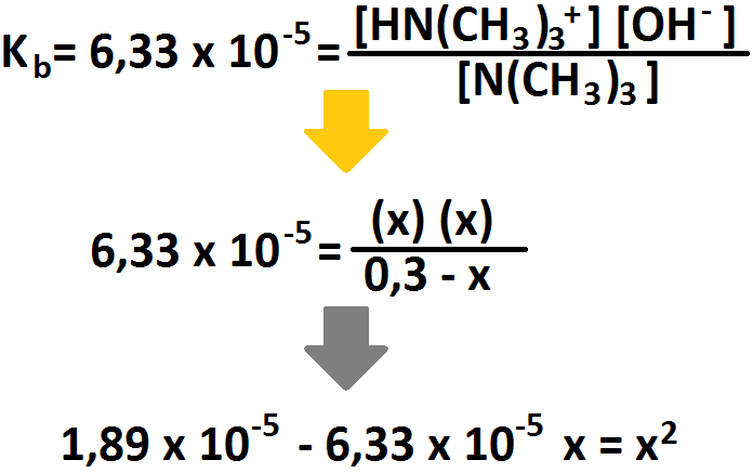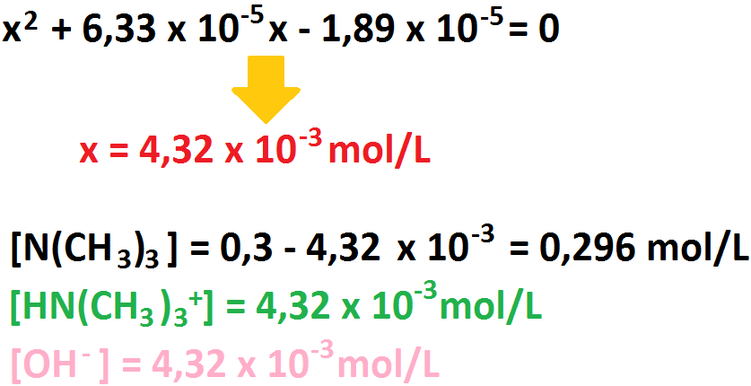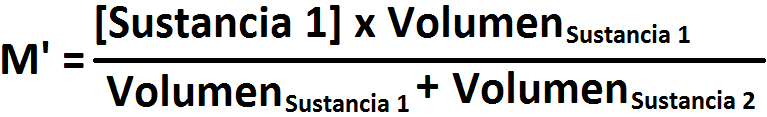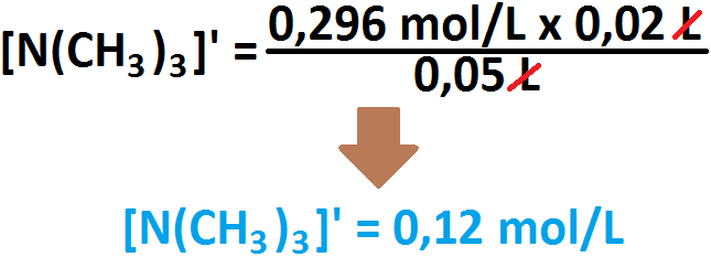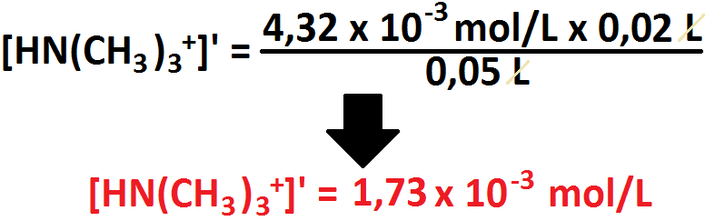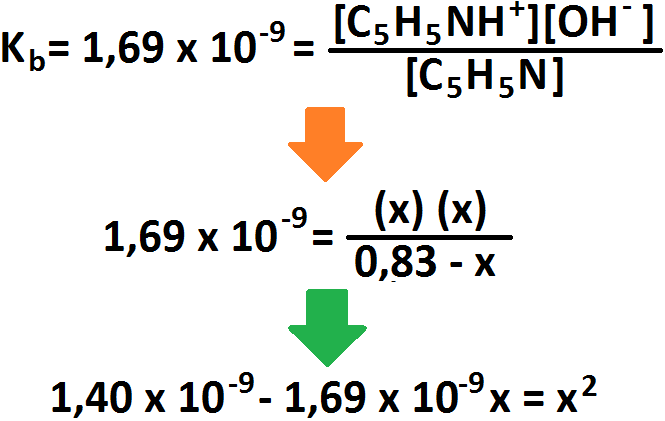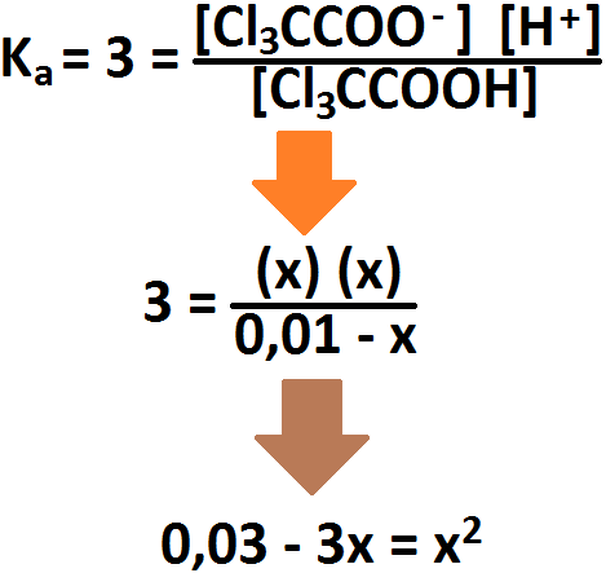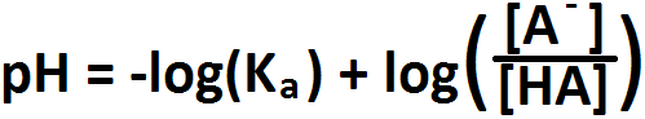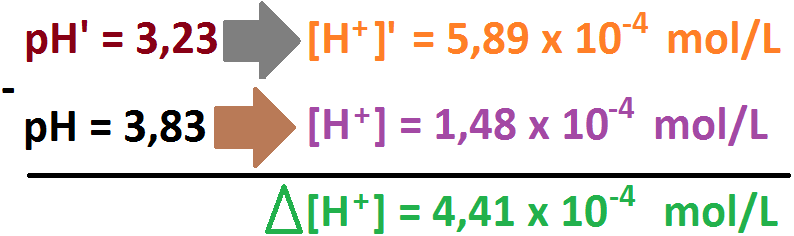Resultados
7.
Como se dijo anteriormente, a partir de ahora, los ejercicios (cuando así sea necesario) se resolverán bajo el método simplificado.
En este ejercicio existe una mezcla de ácidos, uno fuerte (HBr) y uno débil (HF). Primeramente, debemos partir calculando la cantidad de
protones existentes al inicio del problema. Para eso, trabajamos con el pH que se nos ha dado.
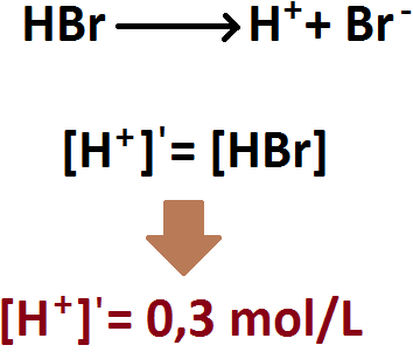
Luego, como sólo tenemos HF en solución, podemos decir que la cantidad de protones que acabamos de calcular corresponde a los
protones aprtados por el ácido débil. Una vez que se añada el ácido fuerte, la cantidad de protones dependerá de ambos ácidos, es
decir, se sumará el aporte de HF con el de HBr. Veamos como nos queda.
Como se puede apreciar, la cantidad de protones aportados por el ácido débil HF es tan pequeña que puede ser despreciada y se
podría considerar solamente el aporte del ácido fuerte para calcular el pH final de la solución. Hagamos eso:
8.
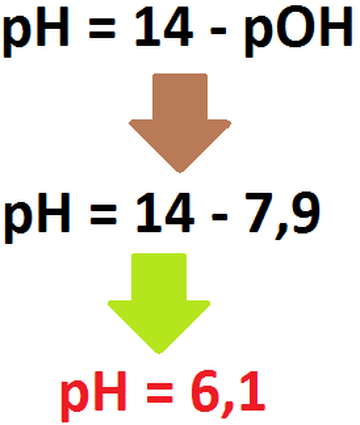
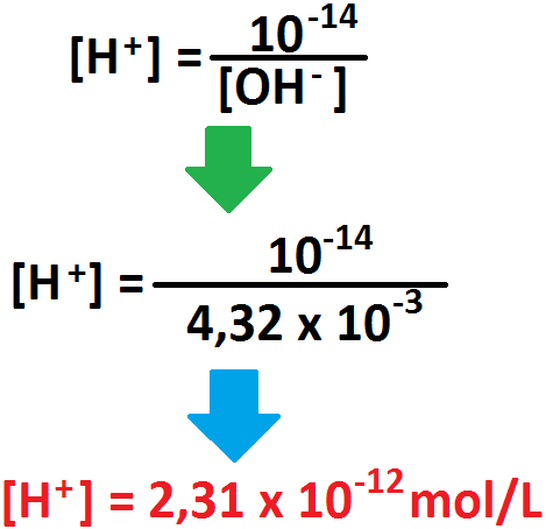
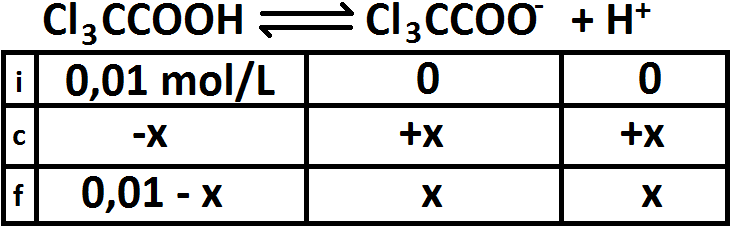
El ácido hidrazoico (HN3) es un ácido débil, por lo cuál no se disocia completamente. Para partir, debemos primeramente saber cuantos
protones tenemos en solución:
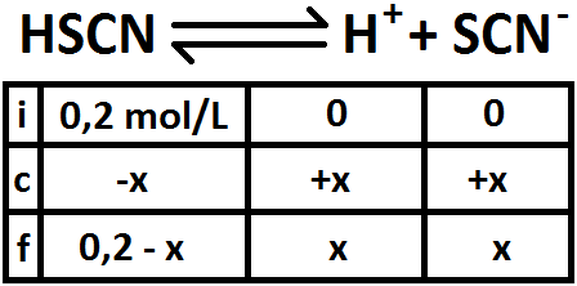
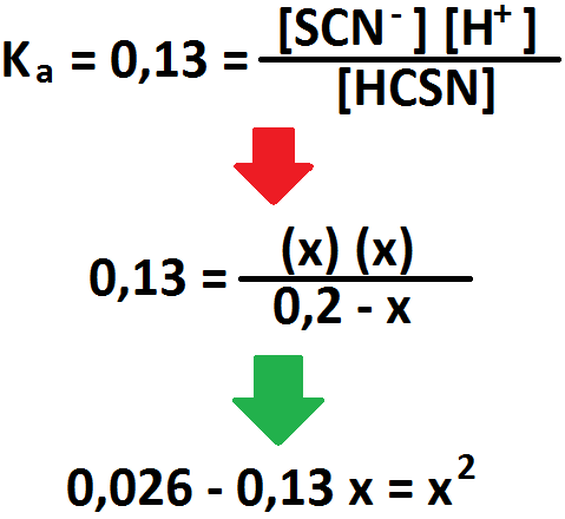
Ahora, hacemos la tabla para averiguar la concentración inicial de ácido:
9.
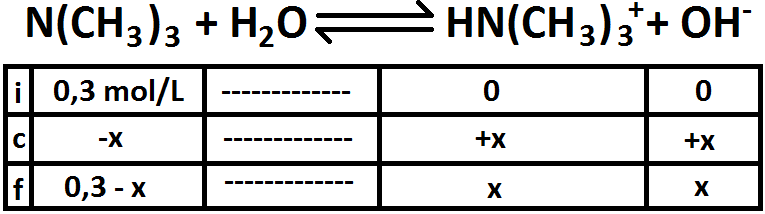
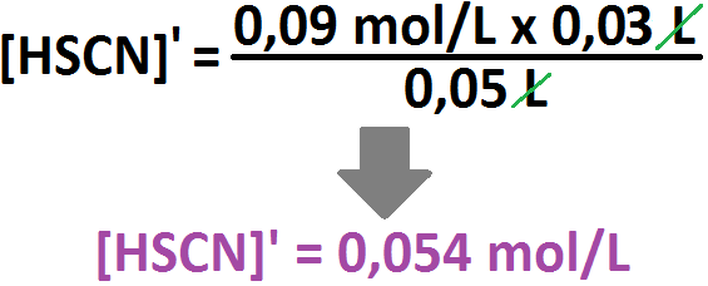
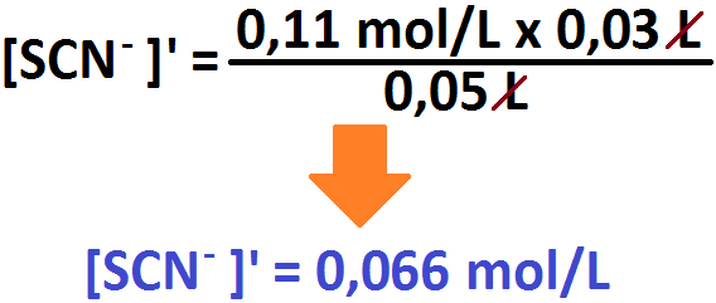
Para desarrollar este ejercicio, primero consideraremos las reacciones por separado. Partamos viendo la del ácido, calculando las concentraciones molares de todas las especies involucradas:
Ahora, hacemos lo mismo con la base:
Luego, el ejercicio nos dice que estas dos disoluciones se mezclan (y que podemos sumar los volúmenes). Cuando esto ocurre, se
nos genera una nueva disolución de un volumen total de 50 mL (30 mL [ó 0,03 L] de la solución ácida y 20 mL [ó 0,02 L] de la solución
básica). Como varió el volumen, también varían las concentraciones molares. Pero antes de hacer esto, calculemos la cantidad de
protones presentes en la solución básica:
Ahora, para poder calcular las nuevas concentraciones molares debe usarse la siguiente fórmula:
En donde, M' representa la nueva concentración molar a ser calculada, Volumensustancia 1 corresponde al volumen inicial de la
sustancia a la que se le calcula la concentración nueva, [Sustancia 1] corresponde a la concentración inicial de la sustancia en cuestión.
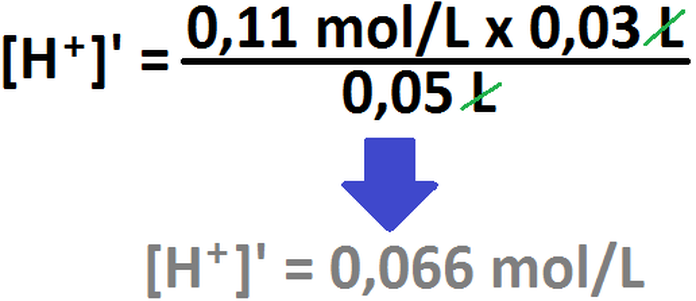
Lo que corresponde al denominador ya lo conocemos (es la suma de los volúmenes, en este caso, 50 mL [ó 0,05 L]). Teniendo esta
fórmula, procedamos al cálculo de las nuevas concentraciones de todas las especies involucradas:
Si comparamos la cantidad de protones que aporta la solución básica y la solución ácida, vemos que la cantidad aportada por esta
última solución es 47.600 millones (aprox.) mayor que la que aporta la primera, por lo cual podemos despreciar los protones aportados
por la solución básica, quedándonos:
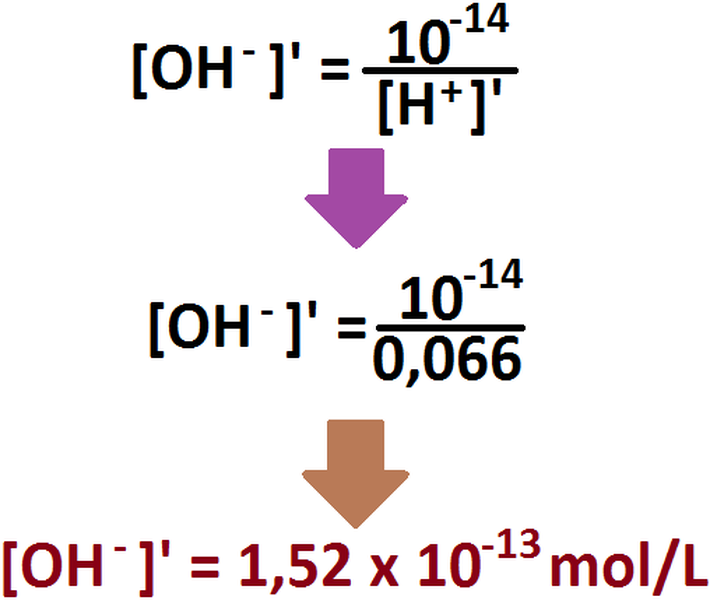
Para finalizar, se calcula la concentración de iones hidroxilo presentes en los 50 mL de solución (claramente ácida):
10.
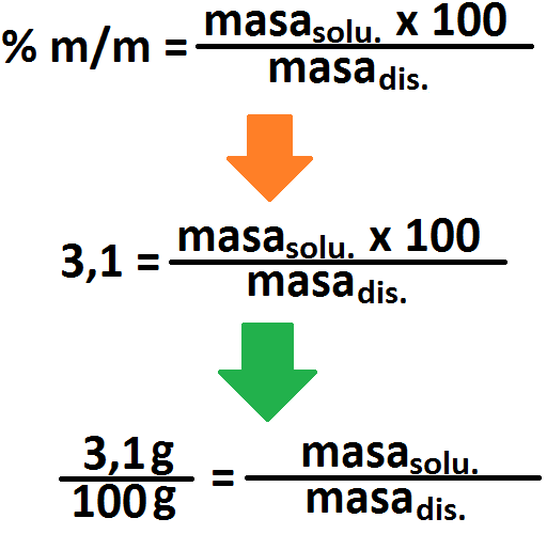
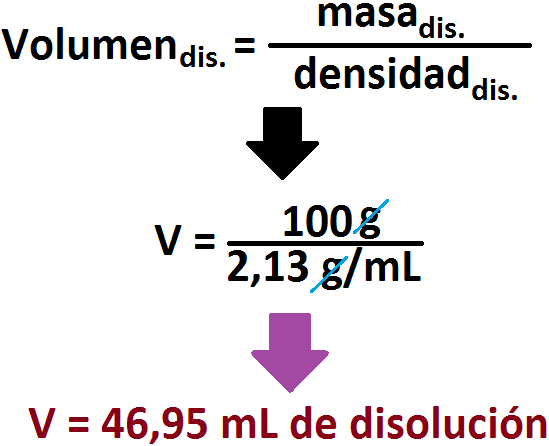
Para hacer este ejercicio, primero debemos calcular la concentración molar de la base inicial (llamada piridina). Para ello, usaremos los
datos que nos entregan (masa molar, %m/m y densidad de la solución):
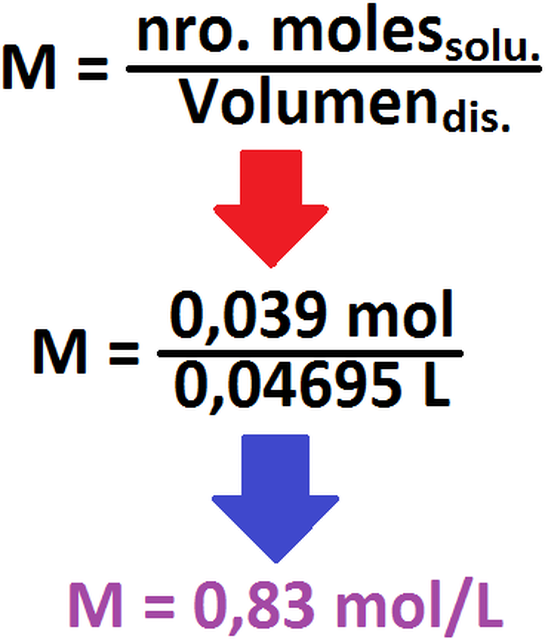
Como se ve arriba, nosotros podemos suponer (debido a que no contamos con esos datos) de que la masa de la base es de 3,1 g y
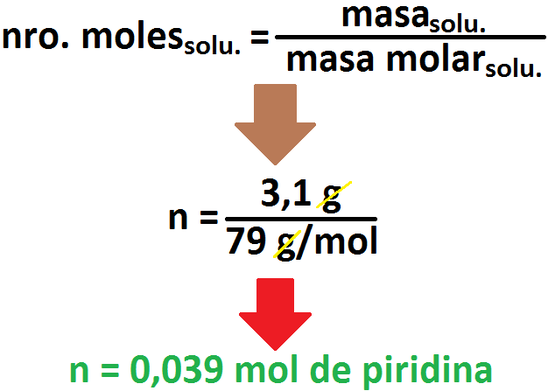
que se encuentra en 100 g de solución. Estos datos nos serán útiles a la hora de calcular la concentración molar del soluto.
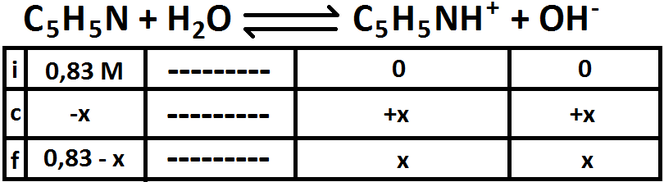
Una vez realizado esto, se procede como para cualquier base débil (haciendo la tabla y todo lo que se realizó anteriormente):
11.
Este ejercicio se desarrolla de una manera similar, que el ejercicio 9, ya que debemos considerar cada reacción por separada primero
y luego juntarlas. Partamos calculando el pH inicial de la primera solución:
Para continuar con el ejercicio, vemos que añadimos una base, por lo cual podemos decir que aumentamos la cantidad iones hidroxilos
en el medio. Cuando esto sucede, los iones hidroxilos se juntan con los protones para formar agua (una neutralización), por lo cual, se
deben restar una cantidad de protones igual a lo que se agrego de iones hidroxilos. Esto no se hizo en el ejercicio 9, debido a que esa
resta daba una concentración de protones muy cercana a 0,11 mol/L, por lo que se omitió. Por eso es necesario saber el número de
iones hidroxilos aportados por la base. Eso es lo que haremos ahora:
Se puede apreciar que esta concentración de iones hidroxilos es aproximadamente 10.000 veces menor que la de protones, por lo que
podríamos omitirla. ¡OJO, NO SE EQUIVOQUEN! Estas no son las concentraciones que debemos restar, acuérdense que al
mezclarlas, creamos una nueva solución con un volumen nuevo y concentraciones nuevas, por lo cual tenemos que re-calcularlas con
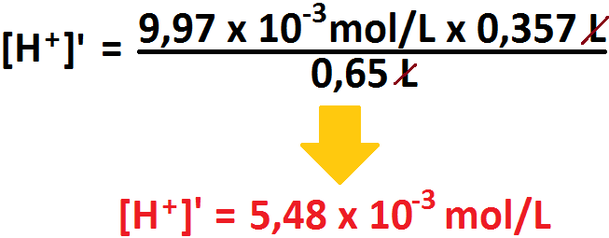
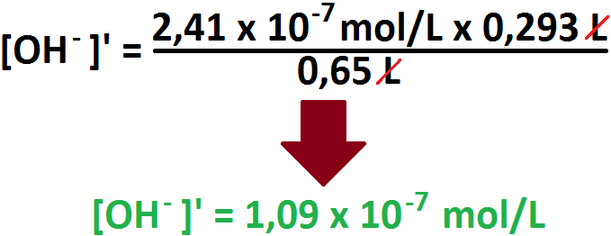
el nuevo volumen, usando la fórmula utilizada en el ejercicio 9 para este fin:
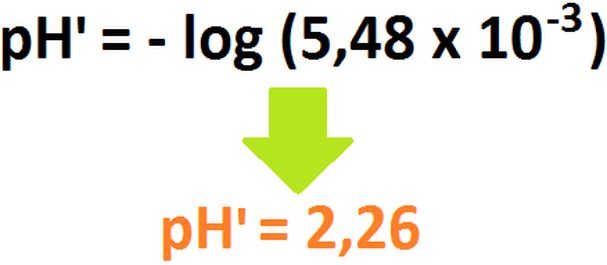
Ahora sí podemos despreciar el gasto de protones necesario para neutralizar los iones hidroxilos, por lo cual podemos calcular el nuevo
pH y sacar la diferencia de éste:
Es decir, finalmente, pasamos de una solución de pH = 2 a otra de pH = 2,26 (por lo tanto, hubo un incremento del pH de 0,26 puntos)
12.
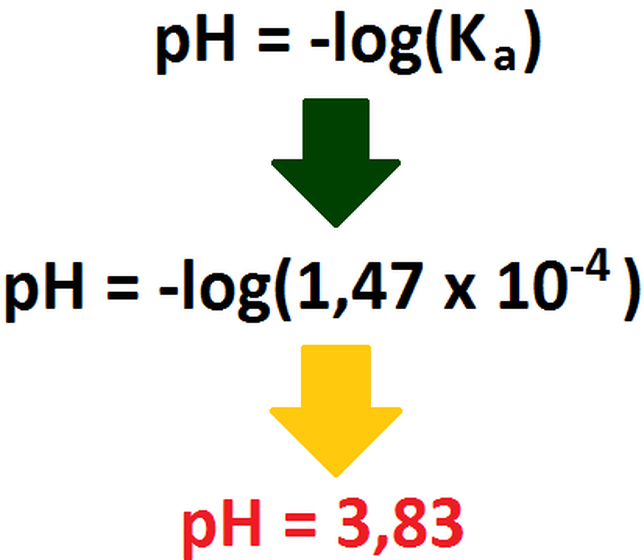
Para hacer este ejercicio, primero debemos calcular el pH inicial de la solución tampón. Para esto se usa la siguiente fórmula:
En donde, HA es la especie ácida protonada (en este caso OHCH2COOH) y A- representa a la base conjugada del ácido (en este caso,
OHCH2COO-). El enunciado del ejercicio nos indica que la razón entre la base conjugada y su ácido es 1:1, por lo que esa división es
igual a 1, y el logaritmo de 1 es siempre 0, por lo que podríamos simplemente decir que, para este caso:
Luego, según el enunciado, una vez que se agregó el ácido hipocloroso (HClO), el pH disminuyó en 0,6 unidades, es decir, quedó un pH
final de 3,23, por ende podemos calcular la cantidad de protones aportadas por el ácido, de la siguiente manera:
Para los que no lo sepan, el triángulo que aparece en verde se llama delta (es la letra mayúscula de la letra griega) y simboliza cambio
o diferencia. Lo que aparece en verde es la cantidad de protones aportados por HClO, y como sabemos su concentración inicial
(0,12 mol/L), podemos sacar su concentración en equilibrio: