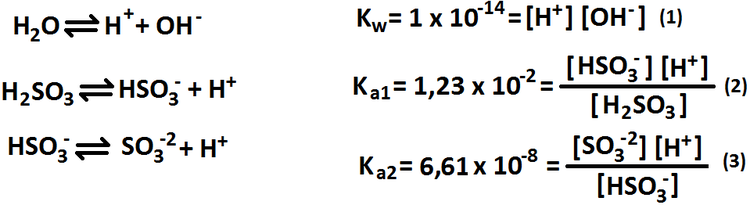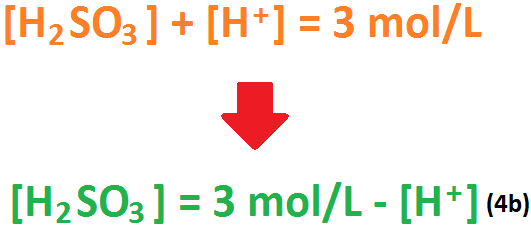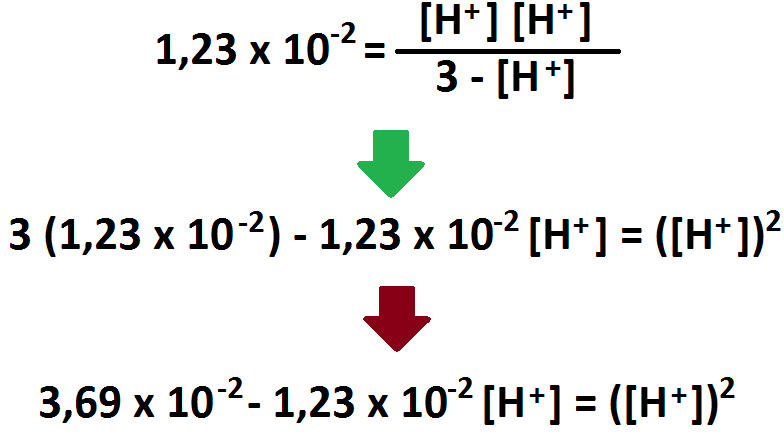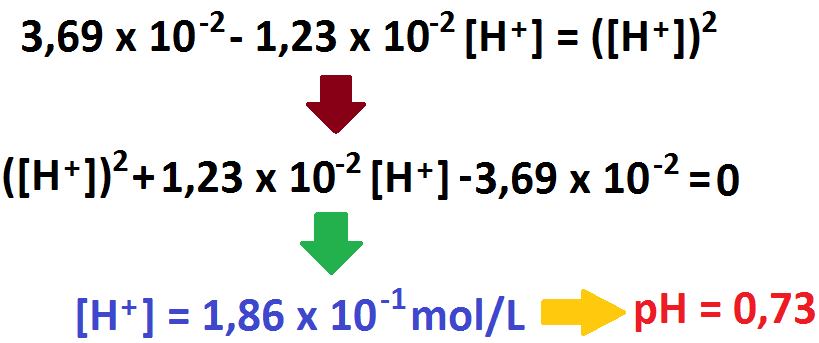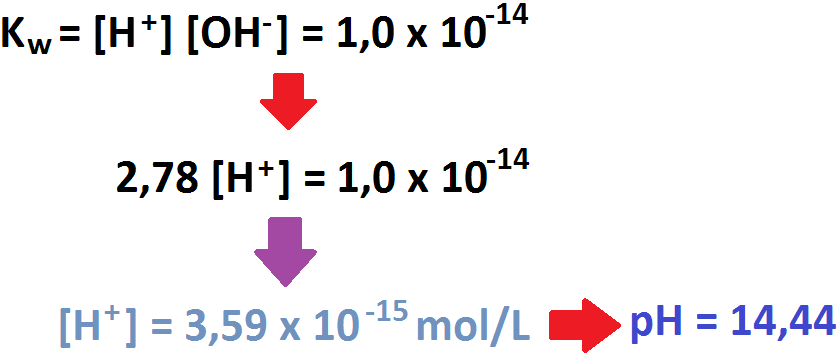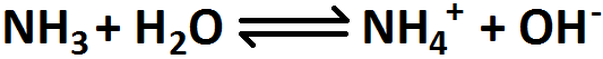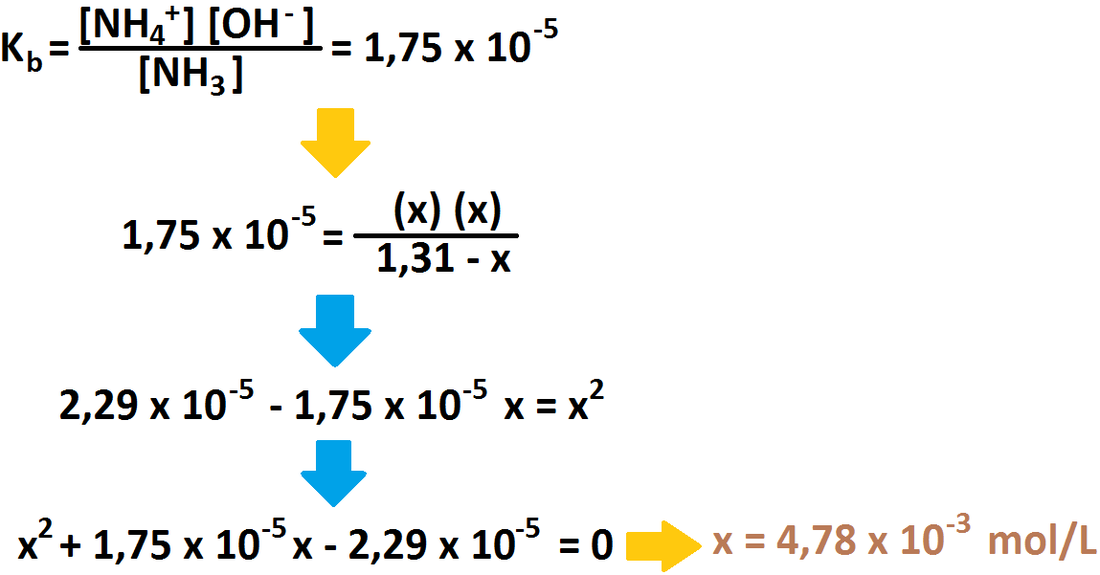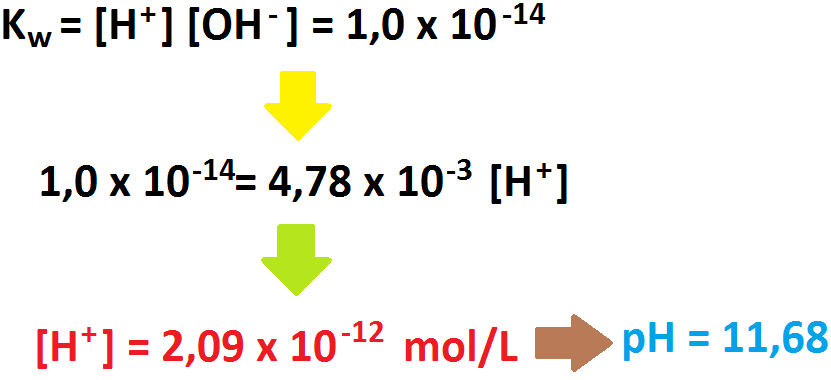Resultados
1.
a) HCl: Ácido de Arrhenius/ Ácido de Lowry-Brönsted. Es un ácido de Arrhenius y de Lowry-Brönsted, debido a que en ambas
definiciones un ácido o bien libera un protón al medio (Arrhenius) o cede un protón a la base (Lowry-Brönsted), es decir,
un ácido tiene un protón en su estructura, tal como lo tiene el HCl.
b) NaOH: Base de Arrhenius. Es una base de Arrhenius, ya que esta es la única teoría que indica que una base libera iones OH- en
medio acuoso, por lo cual la base debiese tener dicho grupo (llamado hidroxilo) en su estructura.
c) HCN: Ácido de Arrhenius/ Ácido de Lowry-Brönsted. Ver la explicación para el HCl, es exactamente la misma.
d) NH3: Base de Lowry-Brönsted/ Base de Lewis. Es una base de Lowry-Brönsted ya que el amoniaco es capaz de captar un protón y
convertirse en ión amonio, mientras que también es considerada una base de Lewis ya que el amoniaco es capaz de compartir
su par electrónico no enlazante (ubicado en el nitrógeno) para poder reaccionar conalguna sustancia deficiente en electrones.
e) Catión Sodio: Ácido de Lewis. Es un ácido de Lewis ya que todos los cationes son especies deficientes de electrones.
f) Anión Bromuro: Base de Lewis. Los aniones son especies que poseen pares de electrones libres, listos pasa ser compartidos, por lo
cuál concuerdan con la definición de una base, según Lewis.
2.
El pH es un valor que se da a una solución para indicar cuán ácida es ésta (mide acidez). Sus valores (más comunes) van desde
0 (cero) hasta14 (aunque pueden haber valores inferiores o superiores).
3.
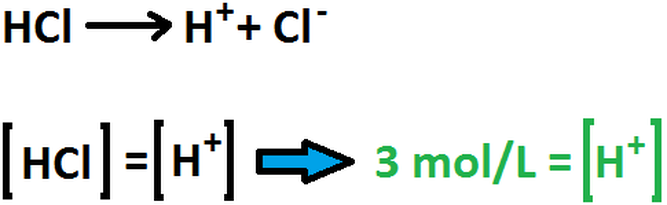
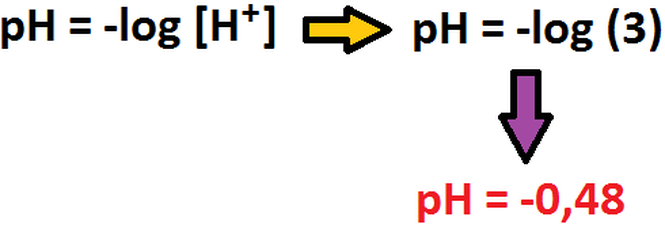
El HCl es un ácido fuerte, por lo cual se disocia completamente en disolución acuosa, por ende, el cálculo del pH se hace directamente:
4.
El ácido sulfuroso es un ácido débil, por lo cual es necesario tener su(s) constante(s) de acidez (en este caso son dos, la primera tiene un valor de 0,0123 y el valor de la segunda constante de acidez es de 0,0000000661). Para el caso de los ácidos y bases débiles, uno puede hacerlo de dos maneras: una simplificada y otra sistemática. Este ejercicio lo desarrollaremos de la primera
Para eso, primero que todo, debemos anotar todas las reacciones involucradas en la disolución y sus constantes respectivas:
Posteriormente, se anotan los balances de masa y carga (para poder cumplir con las leyes de conservación de la masa y de la energía,
respectivamente):
Para simplificar los cálculos, por lo general, se hacen aproximaciones. Cada vez que se haga una aproximación, ésta debe ser verificada
al finalizar el ejercicio (el símbolo >> quiere decir "es mucho mayor que").
Las aproximaciones deben hacerse efectivas en ecuaciones específicas. La aproximación 1 se reemplazará en la ecuación (5), debido a
que es la que nos entrega el aporte del agua a la acidez del medio. Por su parte, la aproximación 2 se hará efectiva en la ecuación (4) y
en la ecuación (5), ya que son en las que aparece la especie a obviar.
Ahora, si reemplazamos la ecuación (5a) en la ecuación (4a), nos quedaría que:
Por último, si reemplazamos la ecuación (4b) y la ecuación (5a) en la ecuación (2), podremos calcular la concentración de protones en
solución y, posteriormente, el pH.
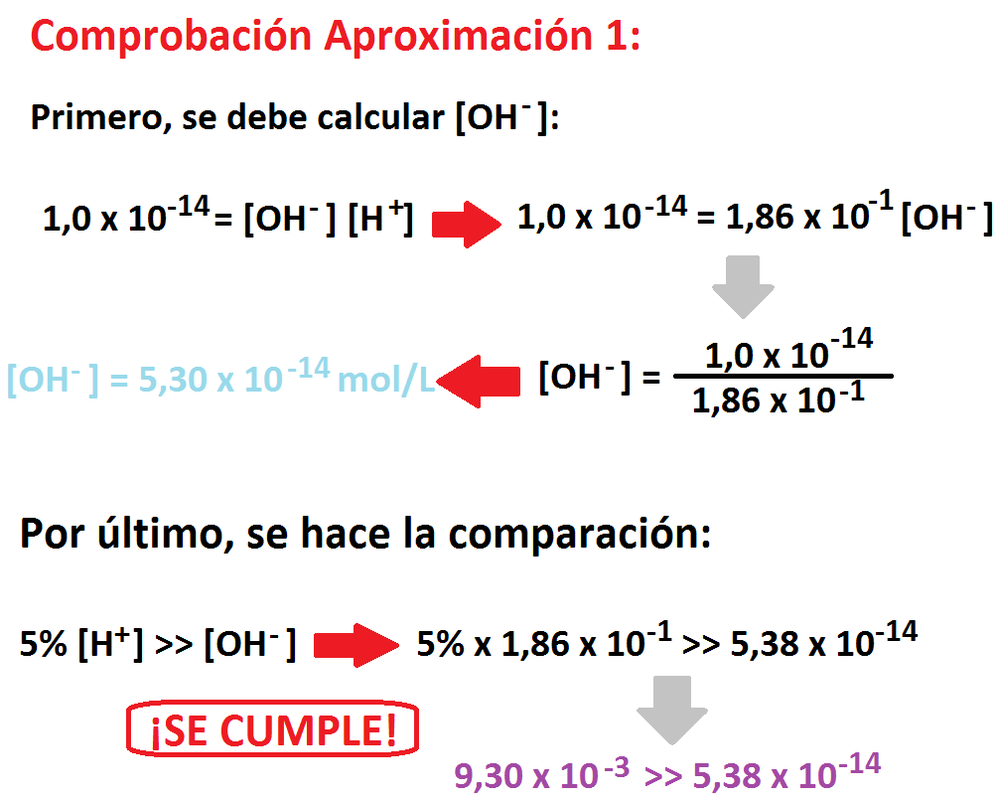
Como se dijo con anterioridad, ahora solo nos falta comprobar las aproximaciones realizadas. De caso de no cumplirse, debe
eliminarse dicha aproximación y volver a hacer los cálculos sin dicha aproximación. Para este ejercicio, las aproximaciones deben
cumplir lo siguiente (y en general, para cualquier aproximación de cualquier ejercicio es igual): el 5% de lo que se dejó debe ser mayor al
valor de la sustancia obviada. Para clarificar, hagamos ésto para nuestras aproximaciones.
Para finalizar, contestaremos la segunda pregunta del ejercicio. Como se puede apreciar, el valor de pH para el ejercicio 3 resultó ser
menor que para este ejercicio ¿Porqué? Esto se debe a que a medida que aumente la concentración de protones, disminuye el pH (este
efecto se debe al signo (-) situado frente al logaritmo). El ejercicio 3 nos pone el caso de un ácido fuerte (HCl), por lo que se disocia
completamente en solución acuosa y deja una mayor cantidad de protones que el H2SO3, que es un ácido débil, es decir, se disocia
parcialmente en solución acuosa.
5.
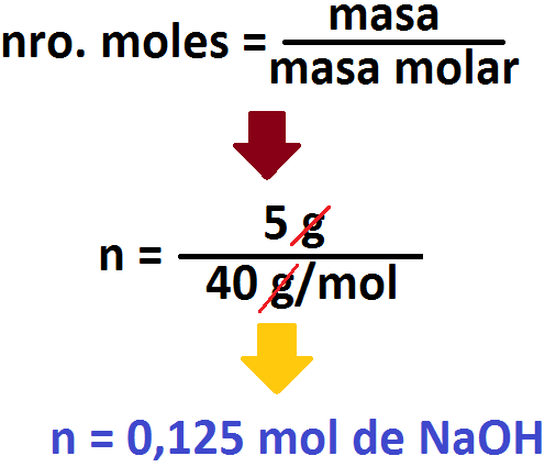
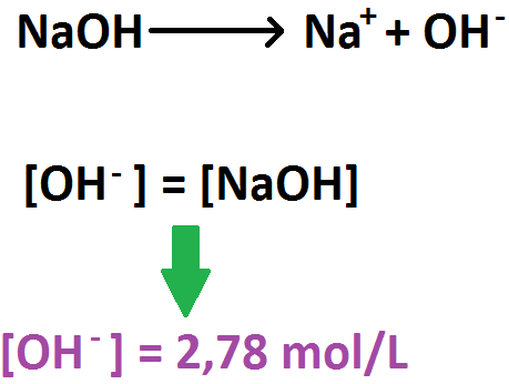
Este ejericicio es similar al ejercicio 3, ya que NaOH es una base fuerte, por lo cual se disocia completamente. Para poder resolverlo,
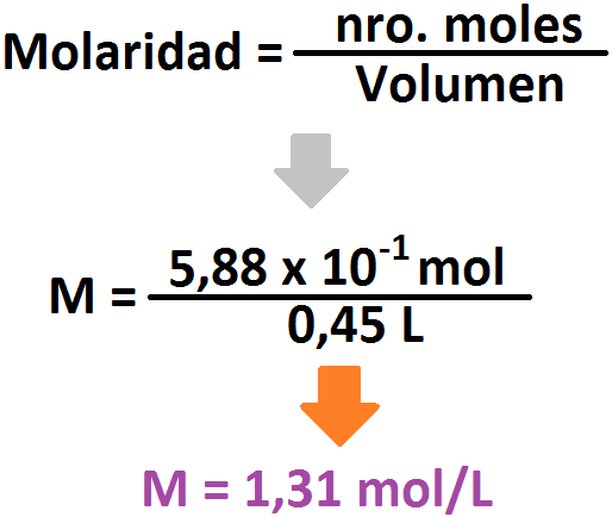
primero debemos calcular cuantos moles de NaOH tenemos en solución:
Luego, sabiendo la cantidad de moles de base y el volumen de solución (45 mL ó 0,045 L), podemos calcular la concentración de NaOH
en solución (2,78 mol/L). Con esto, se nos facilita el poder calcular el pH:
6.
Como el ejercicio 4 se realizó de la manera sistemática, este ejercicio (y los que vengan de aquí en adelante) se harán de la manera
simplificada. Para comprobar de que se obtienen resultados similares, les dejo la tarea de hacer el ejercicio 4, con este método de
resolución. Primero, partimos colocando la ecuación química de la reacción que ocurre cuando se disuelve la base en agua.
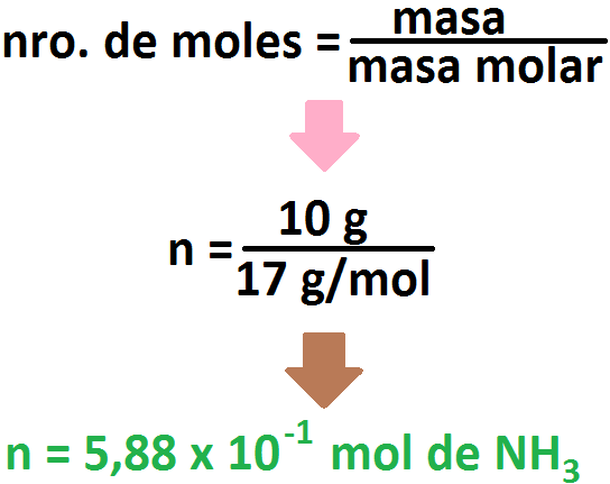
Luego, se calculan las concentraciones iniciales de las sustancias presentes al inicio de la disolución (en este caso, amoniaco y agua).
Como el agua es un líquido, su concentración se mantiene casi igual en todo momento, por lo que no se considerará, razón por la cual,
debiésemos calcular la concentración molar únicamente del amoniaco.
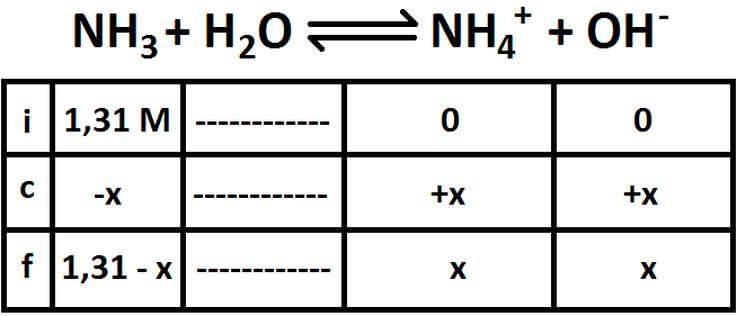
Una vez calculado esto, se hace una tabla de tres filas: una superior (en donde se indica las concentraciones iniciales de las sustan-
cias), una intermedia (donde se indica el cambio de concentraciones) y una inferior (donde se indica las concentraciones finales
una vez alcanzado el equilibrio). Todo esto se ve reflejado a continuación.
Ahora, los valores resultantes de la fila inferior (denominada f) se reemplazan en la constante de basicidad del amoniaco.
Dado lo anterior, podemos decir que la concentración de iones hidroxilos es igual a 0,00478 mol/L, y con este dato es posible calcular
la concentración de protones y, finalmente, el pH de la solución.